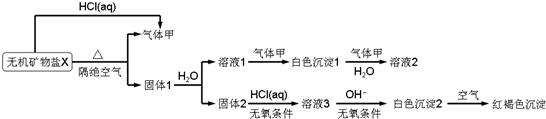
题目内容
用FeCl3酸性溶液脱除H2S后的废液,通过控制电压电解得以再生.某同学使用石墨电极,在不同电压(x)下电解pH=1的0.1mol/L FeCl2溶液,研究废液再生机理.记录如下(a,b,c代表电压值):
(1)用KSCN溶液检测处Fe3+的现象是 .
(2)Ⅰ中Fe3+产生的原因可能是Cl-在阳极放电,生成的Cl2将Fe2+氧化,写出有关反应: .
(3)由Ⅱ推测,Fe3+产生的原因还可能是Fe2+在阳极放电,原因是Fe2+具有 性.
(4)Ⅱ中虽未检验处Cl2,但Cl-在阳极是否放电仍需进一步验证.电解pH=1的NaCl溶液做对照试验,记录如下:
①NaCl溶液的浓度是 mol/L.
②Ⅳ中检验Cl2的实验方法:
③与Ⅱ对比,得出的结论(写出两点): .
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| Ⅰ | x≥a | 电极附近出现黄色,有气泡产生 | 有Fe3+、有Cl2 |
| Ⅱ | a>x≥b | 电极附近出现黄色,无气泡产生 | 有Fe3+,无Cl2 |
| Ⅲ | b>x>0 | 无明显变化 | 无Fe3+,无Cl2 |
(2)Ⅰ中Fe3+产生的原因可能是Cl-在阳极放电,生成的Cl2将Fe2+氧化,写出有关反应:
(3)由Ⅱ推测,Fe3+产生的原因还可能是Fe2+在阳极放电,原因是Fe2+具有
(4)Ⅱ中虽未检验处Cl2,但Cl-在阳极是否放电仍需进一步验证.电解pH=1的NaCl溶液做对照试验,记录如下:
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| Ⅳ | a>x≥c | 无明显变化 | 有Cl2 |
| Ⅴ | c>x≥b | 无明显变化 | 无Cl2 |
②Ⅳ中检验Cl2的实验方法:
③与Ⅱ对比,得出的结论(写出两点):
考点:电解原理,二价Fe离子和三价Fe离子的检验
专题:电化学专题
分析:(1)依据铁离子的检验方法和试剂颜色变化分析;
(2)依据电解原理,氯离子在阳极失电子生成氯气,氯气具有氧化性氧化亚铁离子生成铁离子溶液变黄色;
(3)Fe3+产生的原因还可能是Fe2+在阳极放电,依据氧化还原反应分析Fe2+具有还原性;
(4)①电解pH=1的0.1mol/L FeCl2溶液,电解pH=1的NaCl溶液做对照试验,探究氯离子是否放电,需要在难度相同的条件下进行分析判断;
②依据检验氯气的实验方法分析;
③依据图表数据比较可知,电解pH=1的NaCl溶液做对照试验与Ⅱ对比,通过控制电压证明了亚铁离子还原性大于氯离子优先放电,生成铁离子的两种可能.
(2)依据电解原理,氯离子在阳极失电子生成氯气,氯气具有氧化性氧化亚铁离子生成铁离子溶液变黄色;
(3)Fe3+产生的原因还可能是Fe2+在阳极放电,依据氧化还原反应分析Fe2+具有还原性;
(4)①电解pH=1的0.1mol/L FeCl2溶液,电解pH=1的NaCl溶液做对照试验,探究氯离子是否放电,需要在难度相同的条件下进行分析判断;
②依据检验氯气的实验方法分析;
③依据图表数据比较可知,电解pH=1的NaCl溶液做对照试验与Ⅱ对比,通过控制电压证明了亚铁离子还原性大于氯离子优先放电,生成铁离子的两种可能.
解答:
解:(1)检验铁离子的试剂是硫氰酸钾溶液,用KSCN溶液检测处Fe3+的现象是溶液变红色,故答案为:溶液变红;
(2)依据电解原理,氯离子在阳极失电子生成氯气,电极反应为:2Cl--2e-=Cl2↑,氯气具有氧化性氧化亚铁离子生成铁离子溶液变黄色,反应的离子方程式为:Cl2+2Fe2+=2Fe3++2Cl-;
故答案为:2Cl--2e-=Cl2↑,Cl2+2Fe2+=2Fe3++2Cl-;
(3)由Ⅱ推测,Fe3+产生的原因还可能是Fe2+在阳极放电,元素化合价升高,依据氧化还原反应分析Fe2+具有还原性,故答案为:还原性;
(4)①电解pH=1的0.1mol/L FeCl2溶液,电解pH=1的NaCl溶液做对照试验,探究氯离子是否放电,需要在难度相同的条件下进行,所以氯化钠溶液的浓度为0.2mol/L,故答案为:0.2;
②依据检验氯气的实验方法分析,取少量阳极附近的溶液,滴在淀粉碘化钾试纸上,试纸变蓝色证明生成氯气,否则无氯气生成,
故答案为:取少量阳极附近的溶液,滴在淀粉碘化钾试纸上,试纸变蓝色;
③依据图表数据比较可知,电解pH=1的NaCl溶液做对照试验与Ⅱ对比,通过控制电压证明了亚铁离子还原性大于氯离子优先放电,说明生成铁离子的两种可能,一是二价铁失电子变成三价铁,二是氯离子失电子变成氯气,氯气再氧化二价铁变成三价铁.对于补充的那个实验,实验四的电压高,氯气放电,实验五电压低,氯气不放电,而实验二氯气皆放电;
故答案为:通过控制电压,证实了产生Fe3+的两种原因,通过控制电压,验证了Fe2+先于Cl-放电.
(2)依据电解原理,氯离子在阳极失电子生成氯气,电极反应为:2Cl--2e-=Cl2↑,氯气具有氧化性氧化亚铁离子生成铁离子溶液变黄色,反应的离子方程式为:Cl2+2Fe2+=2Fe3++2Cl-;
故答案为:2Cl--2e-=Cl2↑,Cl2+2Fe2+=2Fe3++2Cl-;
(3)由Ⅱ推测,Fe3+产生的原因还可能是Fe2+在阳极放电,元素化合价升高,依据氧化还原反应分析Fe2+具有还原性,故答案为:还原性;
(4)①电解pH=1的0.1mol/L FeCl2溶液,电解pH=1的NaCl溶液做对照试验,探究氯离子是否放电,需要在难度相同的条件下进行,所以氯化钠溶液的浓度为0.2mol/L,故答案为:0.2;
②依据检验氯气的实验方法分析,取少量阳极附近的溶液,滴在淀粉碘化钾试纸上,试纸变蓝色证明生成氯气,否则无氯气生成,
故答案为:取少量阳极附近的溶液,滴在淀粉碘化钾试纸上,试纸变蓝色;
③依据图表数据比较可知,电解pH=1的NaCl溶液做对照试验与Ⅱ对比,通过控制电压证明了亚铁离子还原性大于氯离子优先放电,说明生成铁离子的两种可能,一是二价铁失电子变成三价铁,二是氯离子失电子变成氯气,氯气再氧化二价铁变成三价铁.对于补充的那个实验,实验四的电压高,氯气放电,实验五电压低,氯气不放电,而实验二氯气皆放电;
故答案为:通过控制电压,证实了产生Fe3+的两种原因,通过控制电压,验证了Fe2+先于Cl-放电.
点评:本题考查了离子检验方法和现象分析,电解原理的分析应用,电解反应,电极产物的理解应用,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
 水是生命之源,2014年我国科学家首次拍摄到水分子团簇的空间取向图象,模型如图所示,下列关于水的说法正确的是( )
水是生命之源,2014年我国科学家首次拍摄到水分子团簇的空间取向图象,模型如图所示,下列关于水的说法正确的是( )| A、水是弱电解质 |
| B、可燃冰是可以燃烧的水 |
| C、氢氧两种元素只能组成水 |
| D、0℃时冰的密度比液态水的密度大 |
下列各组物质中,不满足组内任意两种物质在一定条件下均能发生反应的是( )
| 物质 组别 | 甲 | 乙 | 丙 |
| A | Al | HCl | NaOH |
| B | NH3 | O2 | HNO3 |
| C | SiO2 | NaOH | HF |
| D | SO2 | Ca(OH)2 | NaHCO3 |
| A、A | B、B | C、C | D、D |
下列混合物的分离或提纯操作不正确的是( )
| A、除去N2中的少量O2,可通过灼热的Cu网后,收集气体 |
| B、除去FeCl3溶液中Fe(OH)3沉淀可以过滤 |
| C、重结晶不能用于提纯物质 |
| D、除去KCl中的K2CO3加适量盐酸 |
将2.3g钠放入足量的质量为mg的水中,另将0.1mol镁放入足量的质量为mg的稀硫酸中,反应结束后得两溶液的质量分别为ag和bg,则a g与b g两数的关系应是( )
| A、a>b | B、a=b |
| C、a<b | D、无法确定 |
异戊烷和新戊烷互为同分异构体的依据是( )
| A、分子式相同,但结构不同 |
| B、具有相似的物理性质 |
| C、具有相同的空间结构 |
| D、具有相似的化学性质 |
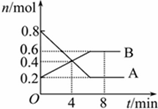 某温度时,在0.5L密闭容器中某一反应的A,B气体物质随时间变化的曲线如图所示,由图中数据分析求得:
某温度时,在0.5L密闭容器中某一反应的A,B气体物质随时间变化的曲线如图所示,由图中数据分析求得: 向一容积不变的密闭容器中充入一定量A和B,发生如下反应:x A(g)+2B(s)?y C(g);△H<0
向一容积不变的密闭容器中充入一定量A和B,发生如下反应:x A(g)+2B(s)?y C(g);△H<0