题目内容
在标准状况下,该反应生成了3.36L氧气,则反应中转移的电子是( )
| A、0.4mol |
| B、0.3NA |
| C、6.02×1022 |
| D、0.2 |
考点:氧化还原反应的计算
专题:氧化还原反应专题
分析:反应2Na2O2+2CO2=2Na2CO3+O2中,只有O元素化合价发生变化,由-1价分别变化为-2价、0价,反应中Na2O2既是氧化剂也是还原剂,结合化合价的变化解答该题.
解答:
解:22.反应2Na2O2+2CO2=2Na2CO3+O2中,只有O元素化合价发生变化,由-1价分别变化为-2价、0价,反应中Na2O2既是氧化剂也是还原剂,
故答案为:C;
23.n(O2)=
=0.15mol,由方程式可知每生成1mol氧气转移2mol电子,则生成0.15mol氧气转移0.3mol电子.
故答案为:B.
故答案为:C;
23.n(O2)=
| 3.36L |
| 22.4L/mol |
故答案为:B.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应中基本概念的考查,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 已知甲、乙、丙、X是4种中学化学中常见的物质,其转化关系符合图.则甲和X(要求甲和X互换后也能符合要求)是( )
已知甲、乙、丙、X是4种中学化学中常见的物质,其转化关系符合图.则甲和X(要求甲和X互换后也能符合要求)是( ) ①Na2CO3溶液和稀盐酸 ②Cl2和Fe ③C和O2 ④SO2和NaOH溶液 ⑤AlCl3溶液和NaOH溶液.
| A、①②③④均可以 |
| B、②③④⑤均可以 |
| C、①②③⑤均可以 |
| D、①③④⑤均可以 |
下列对Na2CO3的叙述不正确的是( )
| A、该物质属于盐类 |
| B、该物质既含金属元素又含非金属元素 |
| C、该物质不能发生化合反应 |
| D、该物质有时候能和NaOH划为一类 |
已知:HCl(aq)与NaOH(aq)反应的△H=-57.3kJ?mol-1,CH3COOH在水中电离的△H=+8.95kJ?mol-1,则CH3COONa水解时的△H为( )
| A、+66.25 kJ?mol-1 |
| B、+48.35 kJ?mol-1 |
| C、-66.25 kJ?mol-1 |
| D、-48.35kJ?mol-1 |
下列各组物质中,属于同分异构体的是( )
| A、O2和O3 |
| B、CH2=CHCH2CH3和CH3CH=CHCH3 |
| C、CH3CH2CH3和CH3(CH2)2CH3 |
| D、CH3CH2OH和CH3OCH3 |
对CH3-CH=CH-C≡C-CF3分子结构的下列叙述中,正确的是( )
| A、6个碳原子有可能都在同一直线上 |
| B、在同一直线上的原子至少有5个 |
| C、在同一平面上的原子至少有8个 |
| D、分子中呈四面体结构的碳原子有3个 |
下列变化中,既属于氧化还原反应又属于吸热反应的是( )
| A、铝和盐酸反应 |
| B、灼热的碳与二氧化碳反应 |
| C、酸碱中和反应 |
| D、氢氧化钡晶体和氯化铵晶体反应 |
对下列事实的解释正确的是( )
| A、蔗糖加入浓硫酸后变黑,说明浓硫酸具有吸水性 |
| B、向50mL18mol?L-1 的H2SO4溶液中加入足量的铜片加热充分反应后,被还原的H2SO4的物质的量小于0.45mol |
| C、常温下,浓H2SO4可以用铝制容器贮存,说明铝与浓H2SO4不反应 |
| D、SO2使高锰酸钾溶液褪色,说明SO2具有漂白性 |
下列化学用语表示正确的是( )
A、HClO的电子式为 |
B、硝基苯的结构简式为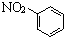 |
| C、饱和醇的通式CnH2n+2O |
D、 表示甲烷分子的球棍模型 表示甲烷分子的球棍模型 |