题目内容
19.分子中含有34个氢原子的烷烃是十六烷(填名称),乙烯的结构简式为CH2=CH2,糖尿病患者尿液中含的糖类的分子式C6H12O6.分析 设烷烃的化学式为CxH2x+2,根据氢原子数求碳原子数,然后根据碳原子数判断其名称;乙烯分子中含有碳碳双键,结构简式中需要标出官能团结构;糖尿病患者尿液中含的糖是葡萄糖,写出葡萄糖的分子式.
解答 解:设烷烃的化学式为CxH2x+2,则2x+2=34,解得x=16,则该烷烃为十六烷;
乙烯分子中含有1个碳碳双键,其结构简式为:CH2=CH2;
糖尿病患者尿液中含的糖类是葡萄糖,葡萄糖中是一个多羟基醛,其分子式为:C6H12O6,
故答案为:十六烷;CH2=CH2;C6H12O6.
点评 本题考查了常见有机物组成、结构与性质,题目难度不大,明确常见有机物结构与性质为解答关键,注意掌握结构简式、分子式等化学用语的书写原则,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
7.在通风橱中进行的关于铁的性质的下列实验:
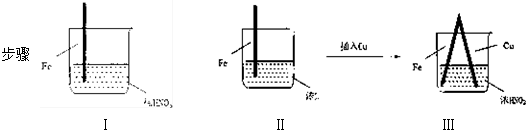
现象依次为ⅠFe表面产生大量无色气泡,液面上方变为红棕色
ⅡFe表面产生少量红棕色气泡后,迅速停止
ⅢFe、Cu接触后,其表面均产生红棕色气泡
下列说法中不正确的是( )

现象依次为ⅠFe表面产生大量无色气泡,液面上方变为红棕色
ⅡFe表面产生少量红棕色气泡后,迅速停止
ⅢFe、Cu接触后,其表面均产生红棕色气泡
下列说法中不正确的是( )
| A. | Ⅰ中气体由无色变红棕色的化学方程式为:2NO+O2═2NO2 | |
| B. | Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应 | |
| C. | 对比Ⅰ、Ⅱ中现象,说明稀HNO3的氧化性强于浓HNO3 | |
| D. | 针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化 |
14.下列化工生产过程中,未涉及氧化还原反应的是( )
| A. | 海带提碘 | B. | 氯碱工业 | ||
| C. | 煅烧石灰石制取生石灰 | D. | 海水提溴 |
4.X、Y、Z是短周期三种元素,它们在周期表中的位置如图所示.试回答:
(1)X元素单质的化学式是He.
(2)Z元素的原子结构示意图为 .
.
(3)Y在元素周期表中的位置是第二周期、ⅤⅡA族.
(4)与Z同主族的下一周期元素的原子序数是34.
| X | ||
| Y | ||
| Z |
(2)Z元素的原子结构示意图为
 .
.(3)Y在元素周期表中的位置是第二周期、ⅤⅡA族.
(4)与Z同主族的下一周期元素的原子序数是34.
11.NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,11.2L的CH2Cl2中所含的分子数为0.5NA | |
| B. | 28g乙烯所含共用电子对数目为4NA | |
| C. | 8.7MnO2与40mL10mL/L的浓盐酸充分反应,生成的氯气分子数小于0.1NA | |
| D. | 1molCaC2中所含阴离子数为2NA |
5.常温下,下列各组离子一定能在指定溶液中大量共存的是( )
| A. | 使酚酞变红色的溶液中:Na+、Fe2+、SO42-、Cl- | |
| B. | 使紫色石蕊试纸变红的溶液中:K+、Fe2+、NO3-、Ca2+ | |
| C. | 常温下PH=12的溶液中:Na+、I-、NO3-、Cl- | |
| D. | 与Al反应放出H2的溶液中:Na+、SO42-、ClO-、Cl- |
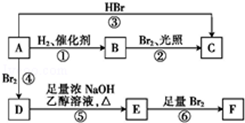 烯烃A在一定条件下可以按下面的框图进行反应.
烯烃A在一定条件下可以按下面的框图进行反应.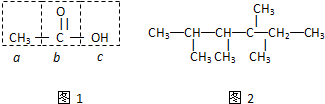
 .
.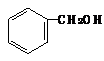 .
.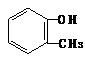 .
.