题目内容
11.NA为阿伏加德罗常数的值,下列说法正确的是( )| A. | 标准状况下,11.2L的CH2Cl2中所含的分子数为0.5NA | |
| B. | 28g乙烯所含共用电子对数目为4NA | |
| C. | 8.7MnO2与40mL10mL/L的浓盐酸充分反应,生成的氯气分子数小于0.1NA | |
| D. | 1molCaC2中所含阴离子数为2NA |
分析 A、标况下二氯甲烷为液态;
B、求出乙烯的物质的量,然后根据1mol乙烯中含6mol共用电子对来分析;
C、二氧化锰只能和浓盐酸反应,和稀盐酸不反应;
D、CaC2中含1个钙离子和1个C22-.
解答 解:A、标况下二氯甲烷为液态,故不能根据气体摩尔体积来计算其物质的量和分子个数,故A错误;
B、28g乙烯的物质的量为1mol,而1mol乙烯中含6mol共用电子对,故含6NA个,故B错误;
C、二氧化锰只能和浓盐酸反应,和稀盐酸不反应,故浓盐酸不能反应完全,则生成的氯气分子小于0.1NA个,故C正确;
D、CaC2中含1个钙离子和1个C22-,故1mol碳化钙中含阴离子为NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
2.下列叙述错误的是( )
| A. | 油脂、淀粉、蔗糖和蛋白质在一定条件能发生水解反应 | |
| B. | 甲烷和苯都不能与溴水、酸性高锰酸钾溶液发生反应,但苯不属于饱和烃 | |
| C. | 甲烷与氯气制备一氯甲烷符合绿色原子经济要求 | |
| D. | 乙烯聚合为聚乙烯高分子材料符合绿色原子经济要求 |
6.有关元素X、Y、Z、D、E的信息如下:
请回答下列问题(用化学用语表示):
(1)X的一种氢化物可用于实验室制取X的单质,其反应的化学方程式为2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(2)比较Y与Z的氢化物的稳定性HCl>H2S(用化学式表示).
(3)E元素与Y元素可形成EY2和EY3两种化合物,则下列说法中正确的是②③(填序号)
①通常实验室配制EY3溶液时,可直接用水溶解EY3固体
②EY2不能通过单质直接化合产生
③铜片、碳棒和EY3溶液组成原电池,电子由铜片沿导线流向碳棒
④Y、Z、D的离子半径大小依次减小
(4)Y的最高价氧化物为无色液体,当0.25mol该物质与一定量的水混合得到一种稀溶液时,放出Q kJ的热量.写出该反应的热化学方程式Cl2O7(l)+H2O(l)═2HClO4(aq)△H=-4QkJ/mol.
(5)写出E在潮湿的空气中发生腐蚀时正极上的电极反应式O2+2H2O+4e-=4OH-.
| 元素 | 有关信息 |
| X | 元素主要化合价-2,原子半径为0.0074nm |
| Y | 所在主族序数与所在周期序数之差为4 |
| Z | 单质在X的单质中燃烧,产物是造成酸雨的罪魁祸首之一 |
| D | 最高价氧化物对应的水化物能电离出电子数相等的阴、阳离子 |
| E | 单质是生活中的常见金属,其制品在潮湿空气中易被腐蚀或损坏 |
(1)X的一种氢化物可用于实验室制取X的单质,其反应的化学方程式为2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(2)比较Y与Z的氢化物的稳定性HCl>H2S(用化学式表示).
(3)E元素与Y元素可形成EY2和EY3两种化合物,则下列说法中正确的是②③(填序号)
①通常实验室配制EY3溶液时,可直接用水溶解EY3固体
②EY2不能通过单质直接化合产生
③铜片、碳棒和EY3溶液组成原电池,电子由铜片沿导线流向碳棒
④Y、Z、D的离子半径大小依次减小
(4)Y的最高价氧化物为无色液体,当0.25mol该物质与一定量的水混合得到一种稀溶液时,放出Q kJ的热量.写出该反应的热化学方程式Cl2O7(l)+H2O(l)═2HClO4(aq)△H=-4QkJ/mol.
(5)写出E在潮湿的空气中发生腐蚀时正极上的电极反应式O2+2H2O+4e-=4OH-.
3.分枝酸的结构简式如图,下列叙述正确的是( )
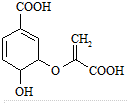

| A. | 分枝酸分子中含有2种官能团 | |
| B. | 分枝酸可与乙醇发生酯化反应 | |
| C. | 分枝酸是芳香族化合物 | |
| D. | 1mol分枝酸最多可与3molNaOH发生反应 |
16.在溶液中能大量共存,加入过量稀盐酸后,溶液中既有沉淀,又有气体产生的离子组是( )
| A. | Cu2+,K+,NO3-,I- | B. | AlO2-,Na+,CO32-,K+ | ||
| C. | Ba2+,Fe3+,Cl-,S2- | D. | K+,SiO32-,S2-,Na+ |
17.图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略).
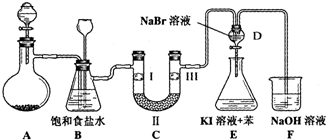
(1)制备氯气选用的药品为:漂粉精固体和浓盐酸,相关的化学反应方程式为:Ca(ClO)2+4HCl(浓)═CaCl2+2Cl2↑+2H2O.
(2)装置B中饱和食盐水的作用是除去Cl2中HCl,贮存少量C12;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象B中长颈漏斗内液面上升,形成一段水柱,锥形瓶内液面下降.
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入D.
(4)设计装置D、E的目的是比较氯、溴、碘的非金属性强弱.打开活塞,将装置D中少量溶液加入装置E中,振荡.观察到的现象是E中溶液分为两层,上层液体为紫红色.
(5)某同学建议将装置F中的药品改用足量的NaHSO3溶液吸收余氯,老师认为不妥,用总反应的离子方程式解释原因4HSO3-+Cl2=SO42-+2Cl-+3SO2+2H2O.

(1)制备氯气选用的药品为:漂粉精固体和浓盐酸,相关的化学反应方程式为:Ca(ClO)2+4HCl(浓)═CaCl2+2Cl2↑+2H2O.
(2)装置B中饱和食盐水的作用是除去Cl2中HCl,贮存少量C12;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象B中长颈漏斗内液面上升,形成一段水柱,锥形瓶内液面下降.
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入D.
| A | B | C | D | |
| Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(5)某同学建议将装置F中的药品改用足量的NaHSO3溶液吸收余氯,老师认为不妥,用总反应的离子方程式解释原因4HSO3-+Cl2=SO42-+2Cl-+3SO2+2H2O.
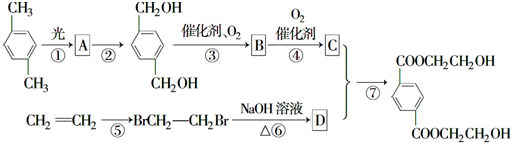
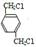 ,B
,B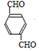 ,
,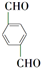 +O2$\stackrel{催化剂}{→}$
+O2$\stackrel{催化剂}{→}$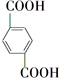
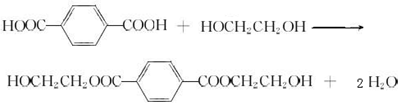
 .
.