题目内容
5.下列物质的变化中,能通过一步化学反应完成的是( )| A. | S→SO3 | B. | Fe→FeCl2 | C. | SiO2→H2SiO3 | D. | Al2O3→Al(OH)3 |
分析 A.S燃烧生成二氧化硫;
B.Fe与盐酸反应生成氯化亚铁和氢气;
C.二氧化硅不溶于水;
D.氧化铝不溶于水.
解答 解:A.S燃烧生成二氧化硫,则不能一步反应生成SO3,故A不选;
B.Fe与盐酸反应生成氯化亚铁和氢气,则Fe$\stackrel{HCl}{→}$FeCl2可一步反应实现,故B选;
C.二氧化硅不溶于水,则不能一步反应生成硅酸,故C不选;
D.氧化铝不溶于水,则不能一步生成氢氧化铝,故D不选;
故选B.
点评 本题考查物质的性质,为高频考点,把握物质的性质、发生的反应为解答该题的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
相关题目
16.生产和生活中,合金几乎无处不在.我国最早使用的合金是( )
| A. | 黄铜 | B. | 铝合金 | C. | 不锈钢 | D. | 青铜 |
13.普罗帕酮为广谱高效抗心律失常药,它可由有机物X经多步反应合成:下列有关说法正确的是( )

| A. | 普罗帕酮分子中有2个手性碳原子 | |
| B. | 可用溴水或FeCl3溶液鉴别X和Y | |
| C. | 在有机物X的1H核磁共振谱图中,有4组特征峰,1mol X 最多可以消耗1mol NaOH | |
| D. | X、Y和普罗帕酮都能发生加成、水解、氧化、消去反应 |
17.氢氧化铝是治疗胃酸过多的内服药的主要成分,这是利用了氢氧化铝的( )
| A. | 弱酸性 | B. | 弱碱性 | C. | 两性 | D. | 不溶解性 |
14.下列叙述不正确的是( )
| A. | 用氢氟酸对玻璃进行刻蚀可制成赏心悦目的雕花玻璃 | |
| B. | Na2CO3粉末遇水生成含有结晶水的碳酸钠晶体,该晶体一定是Na2CO3•10H2O | |
| C. | 氯水和干燥的氯气均能使鲜花褪色 | |
| D. | 合金的硬度可以大于它的纯金属部分,合金的熔点也可以低于它的成分金属 |
15.下列有关实验现象正确的是( )
| A. | 用四氯化碳萃取碘水,下层溶液呈紫色 | |
| B. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- | |
| C. | 往氯化铁溶液中加入氢氧化钠溶液可制得氢氧化铁胶体 | |
| D. | 某溶液滴加紫色石蕊试剂呈红色,该溶液一定含有某种酸 |
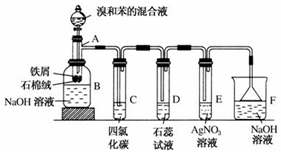 苯和溴的取代反应的实验装置如图所示,其中A为具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑.
苯和溴的取代反应的实验装置如图所示,其中A为具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑.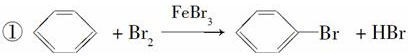 .
.