题目内容
8.试回答下列问题:(1)工业上二氧化硫的催化氧化采用常压而不采用高压的原因是:常压下,三氧化硫的含量已达到91%,从降低成本考虑,没有必要再加压
(2)工业合成氨选择反应条件为500℃的原因是:催化剂催化效率高、反应速率快
(3)工业生产硫酸和氨的工艺中,反应物在接触催化剂之前都必须净化,其目的是:防止催化剂中毒.
分析 (1)常压下三氧化硫的含量已很高,为节约成本,无需增大压强;
(2)对N2(g)+3H2(g)?2NH3(g);△H<0,温度越高越不利于平衡向正方向移动,但在温度角度反应速率较低,不利于反应的进行;
(3)沸腾炉中出来的混合气中含有很多杂质,能够引起催化剂中毒.
解答 解:(1)常压下三氧化硫的含量已很高,为节约成本,无需增大压强,因增大压强,需要增大设备的抗压能力,且消耗能源,
故答案为:常压下,三氧化硫的含量已达到91%,从降低成本考虑,没有必要再加压;
(2)工业合成氨的反应是可逆的,选择500℃左右的较高温度能使反应逆向进行,不利于化学平衡的正向移动,使用该温度主要是考虑催化剂的催化效率以及反应速率等知识,所以工业合成氨选择反应条件为500℃的主要原因是催化剂催化效率高、反应速率快,故答案为:催化剂催化效率高、反应速率快;
(3)沸腾炉中出来的混合气中含有很多杂质,能够引起催化剂中毒,所以防止催化剂中毒,故答案为:防止催化剂中毒.
点评 本题考查工业生产中外界条件的影响,题目难度不大,注意工业生产在环保、安全的基础上以经济效益为中心进行综合分析解答.

练习册系列答案
相关题目
19.将纯锌片和纯铜片按图示方式插入同浓度同体积的稀硫酸中 一段时间,以下叙述正确的是( )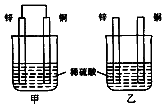

| A. | 两烧杯中铜片表面均无气泡产生 | |
| B. | 两烧杯中溶液的pH均增大 | |
| C. | 甲中电子通过导线由锌片流向铜片,再回到锌片 | |
| D. | 乙中产生气泡的速度比甲快 |
16. 电离平衡常数(用Ka表示)的大小可以判断电解质的相对强弱.25℃时,有关物质的电离平衡常数如下表所示:
电离平衡常数(用Ka表示)的大小可以判断电解质的相对强弱.25℃时,有关物质的电离平衡常数如下表所示:
(1)将浓度为0.1mol/LHF溶液加水稀释一倍(假设温度不变),下列各量减小的是A.
A.c(H+) B.c(H+)•c(OH-) C.c(H+)/c(HF) D.c(OH-)/c(H+)
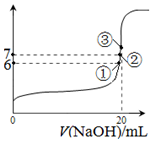
(2)25℃时,在20mL0.1mol•L-1氢氟酸中加入VmL0.1mol•L-1NaOH溶液,测得混合溶液的pH变化曲线如图所示,下列说法正确的是BC.
A.pH=3的HF溶液和pH=11的NaF溶液中,由水电离出的c(H+)相等
B.①点时pH=6,此时溶液中,c(F-)-c(Na+)=9.9×10-7mol/L
C.②点时pH=7,溶液中的c(F-)=c(Na+)
D.③点时V=20mL,此时溶液中c(F-)<c(Na+)=0.1mol•L-1
(3)物质的量浓度均为0.1mol/L的下列四种溶液:①Na2CO3溶液②NaHCO3溶液③NaF溶液④NaClO溶液,pH由大到小的顺序是①>④>②>③(用序号表示).
(4)Na2CO3水解的化学方程式Na2CO3+H2O?NaHCO3+NaOH
(5)简要说明NaHCO3溶液显碱性的原因HCO3-的水解程度大于HCO3-的电离程度.
 电离平衡常数(用Ka表示)的大小可以判断电解质的相对强弱.25℃时,有关物质的电离平衡常数如下表所示:
电离平衡常数(用Ka表示)的大小可以判断电解质的相对强弱.25℃时,有关物质的电离平衡常数如下表所示:| 化学式 | HF | H2CO3 | HClO |
| 电离平衡常数 (Ka) | 7.2×10-4 | K1=4.4×10-7 K2=4.7×10-11 | 3.0×10-8 |
A.c(H+) B.c(H+)•c(OH-) C.c(H+)/c(HF) D.c(OH-)/c(H+)
(2)25℃时,在20mL0.1mol•L-1氢氟酸中加入VmL0.1mol•L-1NaOH溶液,测得混合溶液的pH变化曲线如图所示,下列说法正确的是BC.
A.pH=3的HF溶液和pH=11的NaF溶液中,由水电离出的c(H+)相等
B.①点时pH=6,此时溶液中,c(F-)-c(Na+)=9.9×10-7mol/L
C.②点时pH=7,溶液中的c(F-)=c(Na+)
D.③点时V=20mL,此时溶液中c(F-)<c(Na+)=0.1mol•L-1
(3)物质的量浓度均为0.1mol/L的下列四种溶液:①Na2CO3溶液②NaHCO3溶液③NaF溶液④NaClO溶液,pH由大到小的顺序是①>④>②>③(用序号表示).
(4)Na2CO3水解的化学方程式Na2CO3+H2O?NaHCO3+NaOH
(5)简要说明NaHCO3溶液显碱性的原因HCO3-的水解程度大于HCO3-的电离程度.
3.下列化学反应的速率,前者一定大于后者的是( )
| A. | 相同温度下,颗粒大小相同的锌粒分别与pH值相同的硫酸和盐酸反应 | |
| B. | A+B$\stackrel{500℃}{→}$C;D+E$\stackrel{100℃}{→}$F | |
| C. | 相同温度下,与同浓度盐酸反应的锌粒和铁粉 | |
| D. | G+H→W+Q(Q>0),其他条件相同时分别在200℃和100℃时反应 |
13.中学常用离子检验方法有沉淀法:反应中有沉淀产生或溶解;气体法:反应中有气体产生;显色法:反应中有颜色变化.下列离子检验方法不可能涉及沉淀法的是( )
| A. | NH4+ | B. | Ca2+ | C. | I- | D. | SO42- |
16.(1)一定温度下,Ksp[Mg3(PO3)2]=6.0×10-29,Ksp[Ca3(PO4)2]=6.0×10-26.向浓度均为0.20mol/L的MgCl2和CaCl2混合溶液中逐滴加人Na3PO 4,先生成Mg3(PO4)2沉淀(填化学式);当测得溶液其中一种金属阳离子沉淀完全(浓度小于10-5mol/L)时,溶液中的另一种金属阳离子的物质的量浓度c=10-4mol/L.
(2)毒重石的主要成分BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备BaCl2•2H2O的流程如下:
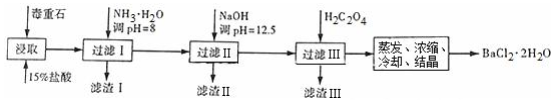
①毒重石用盐酸浸取前需充分研磨,目的是增大接触面积从而使反应速率加快.
②加入NH3•H2O调节PH=8可除去Fe3+(填离子符号),滤渣II中含Mg(OH)2、Ca(OH)2(填化学式).加入H2C2O4时应避免过量,原因是H2C2O4过量会导致生成BaC2O4沉淀,产品的产量减少.
已知:Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9
(3)已知25℃时,CaSO4在水中的沉淀溶解平衡曲线如图所示,向100mL该条件下的CaSO4饱和溶液中加入400mL0.01mol/LNa2SO4溶液,下列叙述正确的是D
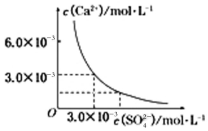
A.溶液中析出CaSO4固体沉淀,最终溶液中c(SO42-)比原来的大
B.溶液中无沉淀析出,溶液中c(Ca2+)、c(SO42-)都变小
C.溶液中析出CaSO4固体沉淀.溶液中c(Ca2+)、c(SO42-)都变小
D.溶液中无沉淀析出,但最终溶液中c(SO42-)比原来的大.
(2)毒重石的主要成分BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备BaCl2•2H2O的流程如下:

①毒重石用盐酸浸取前需充分研磨,目的是增大接触面积从而使反应速率加快.
②加入NH3•H2O调节PH=8可除去Fe3+(填离子符号),滤渣II中含Mg(OH)2、Ca(OH)2(填化学式).加入H2C2O4时应避免过量,原因是H2C2O4过量会导致生成BaC2O4沉淀,产品的产量减少.
| Ca2+ | Mg2+ | Fe3+ | |
| 开始沉淀时的pH | 11.9 | 9.1 | 1.9 |
| 完全沉淀时的pH | 13.9 | 11.1 | 3.7 |
(3)已知25℃时,CaSO4在水中的沉淀溶解平衡曲线如图所示,向100mL该条件下的CaSO4饱和溶液中加入400mL0.01mol/LNa2SO4溶液,下列叙述正确的是D

A.溶液中析出CaSO4固体沉淀,最终溶液中c(SO42-)比原来的大
B.溶液中无沉淀析出,溶液中c(Ca2+)、c(SO42-)都变小
C.溶液中析出CaSO4固体沉淀.溶液中c(Ca2+)、c(SO42-)都变小
D.溶液中无沉淀析出,但最终溶液中c(SO42-)比原来的大.
17.已知某溶液中存在较多的H+、SO42-、NO3-,该溶液中还可能大量存在的离子组是( )
| A. | Na+、NH4+、Cl+ | B. | Mg2+、Ba2+、Br- | C. | Mg2+、Cl-、Fe2+ | D. | K+、SiO32-、Cl- |

 .
.