题目内容
15.一定条件下,分别对反应C(s)+CO2(g)?2CO(g)(正向吸热)进行如下操作(只改变该条件):①升高反应体系的温度;②增加反应物碳的用量;③缩小反应体系的体积;④减少体系中CO的量.上述措施中一定能使反应速率显著变大的是( )| A. | ①②③④ | B. | ①③④ | C. | ①③ | D. | ①② |
分析 常见增大反应速率的因素有浓度、温度、压强、催化剂等,一般来说,增大浓度、压强、升高温度或加入催化剂等都可增大反应速率,以此解答.
解答 解:①升高反应体系的温度,反应速率一定加快,故选;
②C为纯固体,增加反应物C的用量,反应速率不变,故不选;
③缩小反应体系的体积,压强增大,平衡逆向移动,则正逆反应速率均增大,但逆反应速率增大的倍数大,故选;
④减少体系中CO的量,逆反应速率减小,平衡正向移动,但是体系压强降低,反应速率也会减小,故不选;
故选C.
点评 本题考查化学反应速率的影响因素,侧重于学生的分析能力和基础知识的综合理解和运用的考查,难度不大,注意相关基础知识的积累.

练习册系列答案
 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
5.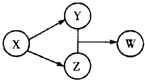 X、Y、Z、W四种物质的转化关系如图所示(部分反应物和产物已经省略).下列组合中不符合该关系的是
X、Y、Z、W四种物质的转化关系如图所示(部分反应物和产物已经省略).下列组合中不符合该关系的是
( )
 X、Y、Z、W四种物质的转化关系如图所示(部分反应物和产物已经省略).下列组合中不符合该关系的是
X、Y、Z、W四种物质的转化关系如图所示(部分反应物和产物已经省略).下列组合中不符合该关系的是 | A | B | C | D | |
| X | HCl | Na2O2 | Na2CO3 | Al2O3 |
| Y | FeCl2 | NaOH | CO2 | AlCl3 |
| Z | Cl2 | Na2CO3 | CaCO3 | NaAlO2 |
| W | FeCl3 | NaHCO3 | Ca(HCO3)2 | Al(OH)3 |
| A. | A | B. | B | C. | C | D. | D |
10.下列化学用语不正确的是( )
| A. | 漂粉精的主要成分:CaCl2 | |
| B. | 乙烯的结构简式:CH2=CH2 | |
| C. | Na+的结构示意图: | |
| D. | 原子核内有10个中子的氧原子:${\;}_{8}^{18}$O |
20.下列反应中,电子转移发生在同种元素之间的是( )
| A. | Fe+Cu2+=Fe2++Cu | B. | 2H2S+SO2=3S+2H2O | ||
| C. | 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ | D. | 2H2O $\frac{\underline{\;电解\;}}{\;}$ 2H2↑+O2↑ |
7.已知I2(g)+H2(g)?2HI(g)△H=-QkJ/mol(Q>0),H-H键能为akJ/mol,H-I键能为bkJ/mol,则I-I键能是( )
| A. | b+Q-a kJ/mol | B. | 2b-Q-a kJ/mol | C. | 2b+Q-a kJ/mol | D. | b-Q+a kJ/mol |
4.25℃,两种酸的电离平衡常数如下表.[已知:Ksp(MnS)=2.8×10-13]
①0.10mol•L-1Na2SO3溶液中离子浓度由大到小的顺序为c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+).
②H2SO3溶液和NaHCO3溶液反应的主要离子方程式为H2SO3+HCO3-=HSO3-+CO2↑+H2O.
| Ka1 | Ka2 | |
| H2SO3 | 1.3×10-2 | 6.3×10-8 |
| H2CO3 | 4.2×10-7 | 5.6×10-11 |
②H2SO3溶液和NaHCO3溶液反应的主要离子方程式为H2SO3+HCO3-=HSO3-+CO2↑+H2O.
5.下列各组离于在溶液中既可以大量共存,且加入氨水后也不产生沉淀的是( )
| A. | Na+ Ba2+ Cl- SO42- | B. | K+ AlO2- NO3-OH- | ||
| C. | H+ NH4 + Al3+ SO42- | D. | H+ Cl- CH3COO- NO3- |



 以氨作为燃料的固体氧化物(含有02-)燃料电池,具有全固态结构、能量效率高、无污染等特点,另外氨气含氢量高,不含碳,易液化,方便运输和贮存,是很好的氢源载体.其工作原理如图所示:
以氨作为燃料的固体氧化物(含有02-)燃料电池,具有全固态结构、能量效率高、无污染等特点,另外氨气含氢量高,不含碳,易液化,方便运输和贮存,是很好的氢源载体.其工作原理如图所示: