题目内容
11.下列关于电解质溶液中离子关系的说法或离子方程式书写正确的是( )| A. | 用铜作电极电解NaCl溶液:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$Cl2↑+H2↑+2OH- | |
| B. | 常温下,向醋酸钠溶液中滴加少量醋酸使溶液的pH=7,则混合溶液中:c(Na+)=c(CH3COO-) | |
| C. | 磷酸一氢钠溶液水解:HPO42-+H2O?PO42-+H3O+ | |
| D. | 常温下,由水电离产生的c(H+)=10-12mol•L-1的溶液,NH4+、SO42-、HCO3-、Cl-能大量共存 |
分析 A、用Cu作电极电解NaCl溶液时,阳极上Cu失电子;
B、根据电荷守恒可知c(H+)+c(Na+)=c(OH-)+c(CH3COO-),结合PH=7综合分析解答;
C、磷酸一氢根离子水解生成磷酸二氢根离子;
D、常温下,由水电离产生的c(H+)=10-12mol•L-1的溶液的pH为2或12.
解答 解:A、用Cu作电极电解NaCl溶液时,阳极上Cu失电子生成铜离子,阴极上氢离子放电生成氢气,故A错误;
B、根据电荷守恒可知c(H+)+c(Na+)=c(OH-)+c(CH3COO-)①,而溶液pH=7,即c(H+)=c(OH-)②,两式相减,得到c(Na+)=c(CH3COO-),故B正确;
C、磷酸一氢根离子水解生成磷酸二氢根离子,HPO42-+H2O?PO42-+H3O+为电离方程式,故C错误;
D、常温下,由水电离产生的c(H+)=10-12mol•L-1的溶液的pH为2或12,HCO3-一定不会大量存在,故D错误;
故选B.
点评 本题考查了电解原理、溶液中的电荷守恒、盐类水解方程式书写、离子共存,属于基础知识的考查,题目难度不大.

练习册系列答案
 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
1.C、H、O三种元素组成的T、X在一定条件下可以发生如下转化: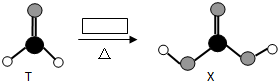
X不稳定,易分解.为使转化能够成功进行,方框内可能加入的试剂是( )

X不稳定,易分解.为使转化能够成功进行,方框内可能加入的试剂是( )
| A. | O2 | B. | NaOH溶液 | C. | 稀硫酸 | D. | Na2SO3溶液 |
2.23g金属钠投入足量水中,反应后生成的气体在标准状况体积为( )
| A. | 22.4 L | B. | 11.2 L | C. | 2 L | D. | 2.5L |
19.对于Zn(s)+H2SO4(aq)═ZnSO4(aq)+H2(g)△H<0 的化学反应,下列叙述错误的是( )
| A. |  反应过程中能量关系可用如图表示 | |
| B. | 若将该反应设计成原电池则锌为负极 | |
| C. | △H的值与反应方程式的化学计量数有关 | |
| D. | 若将其设计为原电池,当有32.5g锌溶解时,转移电子数为2NA |
6.下列说法正确的是( )
| A. | 葡萄糖与果糖、淀粉与纤维素均互为同分异构体 | |
| B. | CH3-CH=CH-CH3与C3H6一定互为同系物 | |
| C. | 甲烷、苯、乙醇、乙酸和酯类都可以发生取代反应 | |
| D. | C3H8的二氯代物共有3种 |
3.下列各组表示式的意义相同的是( )
| A. | -NO2,NO2 | B. | HCOOCH3,CH3OCHO | C. | HCOO-,-COOH | D. | C2H5OH,CH3OCH3 |
9.下列说法不正确的是( )
| A. | 同系物的化学性质相似 | |
| B. | 同位素的化学性质几乎相同 | |
| C. | 相对分子质量相同的化合物,互称同分异构体 | |
| D. | 同素异形体之间的转化,同分异构体之间的转化都属于化学变化 |
10.常温时,在同体积pH=3的HCl、HNO3、CH3COOH溶液中,加入足量镁粉,下列说法正确的是( )
| A. | HCl和HNO3放出H2一样多 | B. | 醋酸中放出H2最多 | ||
| C. | HCl中放出H2最多 | D. | HNO3比醋酸放出H2多 |
 现有A、B、C三种烃,其球棍模型如图:
现有A、B、C三种烃,其球棍模型如图: .
.