题目内容
3.下列物质属于弱电解质的是( )| A. | CH3CH2OH | B. | SO2 | C. | NH3•H2O | D. | HNO3 |
分析 A.CH3CH2OH溶于水不发生电离,属于非电解质;
B.SO2溶于水后自身不发生电离,属于非电解质;
C.NH3•H2O溶于水后部分电离,属于弱电解质;
D.HNO3溶于水后完全电离,属于强电解质.
解答 解:A.CH3CH2OH溶于水不发生电离,属于非电解质,故A错误;
B.SO2溶于水后自身不发生电离,属于非电解质,故B错误;
C.NH3•H2O是弱碱,溶于水后部分电离,属于弱电解质,故C正确;
D.HNO3是强酸,溶于水后完全电离,属于强电解质,故D错误;
故选C.
点评 本题考查了电解质与非电解质、强电解质和弱电解质的区分,题目难度不大,注意掌握基本概念的内涵和外延.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.常温下,浓度均为0.1mol•L-1的4种钠盐溶液pH如下:
下列说法中不正确的是( )
| 溶质 | Na2CO3 | NaHCO3 | NaClO | NaHSO3 |
| pH | 11.6 | 9.7 | 10.3 | 5.2 |
| A. | 四种溶液中,Na2CO3溶液中水的电离程度最大 | |
| B. | 向氯水中加入NaHCO3(s),可以增大氯水中次氯酸的浓度 | |
| C. | NaHSO3溶液显酸性的原因是:NaHSO3═Na++H++SO32- | |
| D. | 常温下,相同物质的量浓度的H2SO3、H2CO3、HClO,pH最小的是H2SO3 |
11.下列判断合理的是( )
①硫酸、烧碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物;
②蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质;
③Na2O、Fe2O3、A12O3属于碱性氧化物
④根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液;
⑤根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应;
⑥CO2、SO2、NO2,都能和碱溶液发生反应,因此它们都属于酸性氧化物.
①硫酸、烧碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物;
②蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质;
③Na2O、Fe2O3、A12O3属于碱性氧化物
④根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液;
⑤根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应;
⑥CO2、SO2、NO2,都能和碱溶液发生反应,因此它们都属于酸性氧化物.
| A. | 只有②④⑥ | B. | 只有①②⑤ | C. | 只有①③⑤ | D. | 只有③④⑥ |
18.铋(Bi)位于元素周期表中ⅤA族,其价态为+3价较稳定,铋酸钠(NaBiO3)溶液呈无色,取一定量的硫酸锰(MnSO4)溶液依次滴加下列溶液,对应的现象如下表所示:
则下列物质的氧化性由弱到强排列的顺序正确的是( )
| 加入溶液 | ①适量铋酸钠溶液 | ②过量的双氧水 | ③适量KI淀粉溶液 |
| 实验现象 | 溶液呈紫红色 | 紫红色消失,产生气泡 | 溶液变成蓝色 |
| A. | I2,H2O2,KMnO4,NaBiO3 | B. | H2O2,I2,NaBiO3,KMnO4 | ||
| C. | NaBiO3,KMnO4,H2O2,I2 | D. | KMnO4,NaBiO3,I2,H2O2 |
15. 如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测.下列说法不正确的是( )
如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测.下列说法不正确的是( )
 如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测.下列说法不正确的是( )
如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测.下列说法不正确的是( )| A. | 电流由O2所在的铂电极流出 | |
| B. | 该电池的负极反应式为:CH3CH2OH+3H2O-12e-═2CO2↑+12H+ | |
| C. | O2所在的铂电极处发生还原反应 | |
| D. | 微处理器通过检测电流大小而计算出被测气体中酒精的含量 |
 实验室制备溴乙烷(C2H5Br)的装置和步骤如下:(已知溴乙烷的沸点38.4℃)①检查装置的气密性,向装置图所示的∪形管和大烧杯中加入冰水;②在圆底烧瓶中加入10mL95%乙醇、28mL78%浓硫酸,然后加入研细的13g溴化钠和几粒碎瓷片;③小心加热,使其充分反应.回答下列问题:
实验室制备溴乙烷(C2H5Br)的装置和步骤如下:(已知溴乙烷的沸点38.4℃)①检查装置的气密性,向装置图所示的∪形管和大烧杯中加入冰水;②在圆底烧瓶中加入10mL95%乙醇、28mL78%浓硫酸,然后加入研细的13g溴化钠和几粒碎瓷片;③小心加热,使其充分反应.回答下列问题: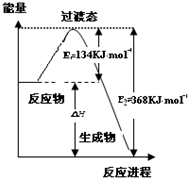 研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
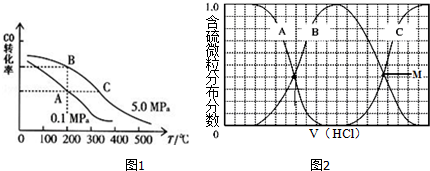
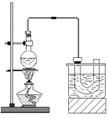
研究NO2、SO2、CO等大气污染气体的处理具有重要意义.