题目内容
20.某MgCl2溶液的密度为1.20g•mL-1,其中Mg2+的质量分数为5%,则300mL该溶液中Cl-的物质的量等于( )| A. | 0.37 mol | B. | 1.5 mol | C. | 0.63 mol | D. | 0.74 mol |
分析 根据c=$\frac{1000ρω}{M}$计算出镁离子的物质的量浓度,然后根据氯化镁的化学式计算出该溶液中氯离子的物质的量浓度,再根据n=cV计算出氯离子的物质的量.
解答 解:该溶液中镁离子的物质的量浓度为:c(Mg2+)=$\frac{1000×1.20×5%}{24}$mol/L≈2.5mol/L,
根据化学式MgCl2的组成可知,c(Cl-)=2c(Mg2+)=2.5mol/L×2=5mol/L,
则300mL该氯化镁溶液中含有氯离子的物质的量为:5mol/L×0.5L=1.5mol
故选B.
点评 本题考查了物质的量浓度的计算,题目难度中等,明确溶质浓度与含有离子浓度的关系为解答关键,注意熟练掌握物质的量浓度与溶质质量分数的关系,试题培养了学生的化学计算能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.已知:①A+B2+═A2++B ②D+2H2O═D(OH)2+H2↑ ③以B、E为电极与E的盐溶液组成原电池,电极反应为:E2++2e-=E,B-2e-═B2+,下列说法正确的是( )
| A. | 氧化性:E2+>B2+>A2+>D2+ | |
| B. | 氧化性:D2+>E2+>A2+>B2+ | |
| C. | 反应E+A2+=A+E2+能够进行 | |
| D. | 提取某废水中含有少量的A2+时可以选用D |
8.列各混合物中,用分液漏斗不能分开的是( )
| A. | .苯与水 | B. | .煤油和乙醇 | C. | 食用油和水 | D. | .乙醇和水 |
15.下列说法中正确的是( )
| A. | 2 mol CH4的质量和O2的摩尔质量都是32g | |
| B. | 1 mol任何气体中都含有相同的原子数 | |
| C. | 1 mol NaCl中含有6.02×1023个微粒 | |
| D. | H3PO4的摩尔质量是98.0g/mol |
5.已知:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H1=-890.3kJ•mol-1;
H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H2=-285.8kJ•mol-1.
CO2与H2反应生成甲烷气体与液态水的热化学方程式为CO2(g)+4H2(g)═CH4(g)+2H2O(l)△H3,则△H3为( )
H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H2=-285.8kJ•mol-1.
CO2与H2反应生成甲烷气体与液态水的热化学方程式为CO2(g)+4H2(g)═CH4(g)+2H2O(l)△H3,则△H3为( )
| A. | -252.9 kJ•mol-1 | B. | +252.9 kJ•mol-1 | C. | -604.5 kJ•mol-1 | D. | +604.5 kJ•mol-1 |
12.下列关于官能团的叙述或书写错误的是( )
| A. | 醇的官能团是羟基(-OH) | B. | 烯烃的官能团碳碳双键 | ||
| C. | 甲醛的官能团是醛基(-COH) | D. | 酚的官能团是羟基(-OH) |
9.短周期主族元素X、Y、Z、W的原子序数依次增大,它们的最外层电子数之和为22,Y的单质广泛用作半导体材料,Z原子的最外层电子数是最内层电子数的3倍.下列说法不正确的是( )
| A. | 原子半径:r(Y)>r(Z)>r(W) | |
| B. | 简单气态氢化物的热稳定性:Y<Z | |
| C. | 氧化物的水化物的酸性:Z<W | |
| D. | X的简单氢化物与W的氢化物相遇可产生白烟 |
10.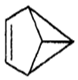 盆烯是近年合成的一种有机物,它的分子结构可简化表示为(其中C、H原子已略去),下列关于盆烯的说法中正确的是( )
盆烯是近年合成的一种有机物,它的分子结构可简化表示为(其中C、H原子已略去),下列关于盆烯的说法中正确的是( )
 盆烯是近年合成的一种有机物,它的分子结构可简化表示为(其中C、H原子已略去),下列关于盆烯的说法中正确的是( )
盆烯是近年合成的一种有机物,它的分子结构可简化表示为(其中C、H原子已略去),下列关于盆烯的说法中正确的是( )| A. | 盆烯是乙烯的一种同系物 | |
| B. | 盆烯分子中所有的碳原子可能在同一平面上 | |
| C. | 盆烯和苯的不属于同分异构体 | |
| D. | .盆烯在一定条件下可以发生加成反应 |
