题目内容
20.下列叙述正确的是( )| A. | 呈酸性的雨水通常称为酸雨 | |
| B. | 翡翠、玛瑙、水晶等饰物都是硅酸盐制品 | |
| C. | 合金材料一定全部由金属元素组成 | |
| D. | 硅是制作太阳能电池的主要原料 |
分析 A、PH小于5.6;
B、水晶的主要成分是二氧化硅,二氧化硅是氧化物不是盐;
C、合金是指在一种金属中加热熔合其它金属或非金属而形成的具有金属特性的物质;
D、硅是半导体.
解答 解:A、PH小于5.6,而不是呈酸性的雨水,故A错误;
B、水晶的主要成分是二氧化硅,二氧化硅是氧化物不是盐,故B错误;
C、合金可以是金属元素与非金属元素组成的,故C错误;
D、硅是半导体,硅是制造太阳能电池的主要原料,故D正确;
故选D.
点评 本题主要考查了物质的用途,掌握物质的性质是解题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.下列化工生产过程中,未涉及氧化还原反应的是( )
| A. | 侯式制碱法制纯碱 | B. | 海带提碘 | ||
| C. | 氯碱工业 | D. | 海水提溴 |
11.下列关于物质的量浓度表述正确的是( )
| A. | 0.3mol•L-1 的Na2SO4溶液中含有Na+和SO42-的总物质的量为0.9mol | |
| B. | 当1L水吸收22.4L氨气时所得氨水的浓度不是1mol•L-1,只有当22.4L氨气溶于水制得1L氨水时,其浓度是1mol•L-1 | |
| C. | 在K2SO4和NaCl的混合溶液中,如果Na+和SO42-的物质的量相等,则K+和Cl-的物质的量浓度一定相同 | |
| D. | 250g胆矾溶于水得到1L溶液,所得CuSO4溶液的物质的量浓度为1mol•L-1 |
8.某无色溶液能与铝作用生成氢气,则溶液中可能大量共存的离子组是:( )
| A. | H+、Ba2+、Mg2+、Cl- | B. | Cl-、CO32-、Cu2+、Mg2+ | ||
| C. | NO3-、SO42-、K+、H+ | D. | NO3-、OH-、Ba2+、Cl- |
12.在强酸性溶液中能大量共存的无色透明离子组是( )
| A. | K+、Na+、NO3-、MnO4- | B. | K+、Na+、Cl-、SO42- | ||
| C. | K+、Na+、Cl-、Cu2+ | D. | Na+、Ba2+、OH-、SO42- |
9.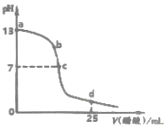 如图为常温下0.2000mol•L-1 CH3COOH溶液逐滴加入到25mL0.1000mol•L-1 NaOH溶液中pH的变化曲线,下列说法不正确的是( )
如图为常温下0.2000mol•L-1 CH3COOH溶液逐滴加入到25mL0.1000mol•L-1 NaOH溶液中pH的变化曲线,下列说法不正确的是( )
 如图为常温下0.2000mol•L-1 CH3COOH溶液逐滴加入到25mL0.1000mol•L-1 NaOH溶液中pH的变化曲线,下列说法不正确的是( )
如图为常温下0.2000mol•L-1 CH3COOH溶液逐滴加入到25mL0.1000mol•L-1 NaOH溶液中pH的变化曲线,下列说法不正确的是( )| A. | a~c区间内(不包含a、c两点)可能存在:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) | |
| B. | c点时溶液中:c(Na+)=c(CH3COO-) | |
| C. | d点时溶液中:c(Na+)+c(H+)+c(CH3COO-)-c(OH-)=0.2000mol•L-1 | |
| D. | 反应过程中溶液中阴、阳离子总数:b点小于c点 |
10.下列反应不能体现乙烯含有不饱和的碳碳双键的是( )
| A. | 乙烯与H2反应 | B. | 乙烯燃烧 | ||
| C. | 乙烯与溴水反应 | D. | 乙烯在催化作用下生成聚乙烯 |