��Ŀ����
6���״���CH3OH����һ����Ҫ�Ļ���ԭ�ϣ���;�dz��㷺����1����ҵ�Ͽ���ʹ��CO��H2��Ӧ���ɼ״���Һ�壩��H2��ȼ����Ϊ-285.8kJ/mol��CO��ȼ����Ϊ-282.8kJ/mol���״���ȼ����Ϊ 726.51kJ/mol������CO��H2���ɼ״����Ȼ�ѧ����ʽΪCO��g��+2H2��g��=CH3OH��l����H=-127.89kJ/mol��
��2��һ���¶��£���2L���ܱ�������Ͷ��1mol CO ��3mol H2������Ӧ���ɼ״������壩��2min��ﷴӦ�ȣ����ѹǿ�Ƿ�Ӧǰ��70%�����ü״���ʾ�ķ�Ӧ����Ϊ0.15mol/��L��min����
���������˵����Ӧ�ﵽ�ȵ���CE��
A����������ܶȲ��ı�
B����λʱ������0.1mol CH3OH��ͬʱ����0.1mol CO
C���������ƽ������������
D���������������
E��v����CO����v����H2��=1��2
�ı��������ܷ�ʹ��Ӧ�ﵽ��ʱ����ϵѹǿΪ��ʼѹǿ��40%������ܡ����ܡ�������Ҫ˵��ԭ���ܣ���Ϊ�÷�ӦΪ���淴Ӧ����CO��ȫ��Ӧʱ��ѹǿΪ��Ӧǰ��50%����˲����ܴﵽ40%��
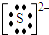
��3���״����Ʒ�Ӧ���ɼ״��ƺ�������д���״��Ƶĵ���ʽ��Na+[
 ]-��
]-����4����ѧ���������Լ״�Ϊȼ�ϵ�ȼ�ϵ�أ��������ΪKOH�����طŵ�ʱ�����ĵ缫��ӦʽΪCH3OH-6e-+8OH-=CO32-+6H2O��
���� ��1��COȼ�յ��Ȼ�ѧ����ʽΪ��CO��g��+$\frac{1}{2}$O2��g���TCO2��g����H=-282.8 kJ/mol��
H2ȼ�յ��Ȼ�ѧ����ʽΪ��H2��g��+$\frac{1}{2}$O2��g���TH2O��g����H=-285.8kJ/mol
CH3OH��l��+$\frac{3}{2}$O2��g���TCO2��g��+2H2O��l����H=-725.8 kJ•mol-1�����ݸ�˹������дCO���������ɼ״����Ȼ�ѧ����ʽ��
��2��2min��ﷴӦ�ȣ����ѹǿ�Ƿ�Ӧǰ��70%��˵����Ӧ���������ʵ����Ƿ�Ӧǰ��70%����Ӧ���������ʵ���=��1+3��mol��70%=2.8mol������CO��g��+2H2��g��=CH3OH��g��֪�����ɼ״������ʵ���=$\frac{4mol-2.8mol}{2}��1$=0.6mol������v=$\frac{\frac{��n}{V}}{��t}$����״��ķ�Ӧ���ʣ�
���淴Ӧ�ﵽƽ��״̬ʱ���淴Ӧ������ȣ���Ӧ��ϵ�и����ʵ����ʵ��������ʵ���Ũ�ȼ��ٷֺ������䣻
���CO��ȫ��Ӧ����Ӧ��������������ʵ���Ϊ2mol��Ϊ��Ӧǰ��50%��
��3���״����ǻ�����ԭ�ӱ�������ȡ�����ɼ״��ƣ�Ϊ���ӻ����
��4�������ϼ״�ʧ���Ӻ����������ӷ�Ӧ����̼������Ӻ�ˮ��
��� �⣺��1��COȼ�յ��Ȼ�ѧ����ʽΪ��CO��g��+$\frac{1}{2}$O2��g���TCO2��g����H=-282.8 kJ/mol�٣�
H2ȼ�յ��Ȼ�ѧ����ʽΪ��H2��g��+$\frac{1}{2}$O2��g���TH2O��g����H=-285.8kJ/mol��
CH3OH��l��+$\frac{3}{2}$O2��g���TCO2��g��+2H2O��l����H=-725.8 kJ•mol-1��
������ʽ��+2��-�۵�CO��g��+2H2��g��=CH3OH��l����H=-127.89 kJ/mol���ʴ�Ϊ��CO��g��+2H2��g��=CH3OH��l����H=-127.89 kJ/mol��
��2��2min��ﷴӦ�ȣ����ѹǿ�Ƿ�Ӧǰ��70%��˵����Ӧ���������ʵ����Ƿ�Ӧǰ��70%����Ӧ���������ʵ���=��1+3��mol��70%=2.8mol������CO��g��+2H2��g��=CH3OH��g��֪�����ɼ״������ʵ���=$\frac{4mol-2.8mol}{2}��1$=0.6mol���״���Ӧ����v=$\frac{\frac{��n}{V}}{��t}$=$\frac{\frac{0.6mol}{2L}}{2min}$=0.15 mol/��L��min����
���淴Ӧ�ﵽƽ��״̬ʱ���淴Ӧ������ȣ���Ӧ��ϵ�и����ʵ����ʵ��������ʵ���Ũ�ȼ��ٷֺ������䣻
A�������������ʼ�ղ��䡢����������䣬���Ի�������ܶ�ʼ�ղ��ı䣬���ܾݴ��ж�ƽ��״̬���ʴ���
B�������Ƿ�ﵽƽ��״̬����λʱ������0.1mol CH3OH��ͬʱ����0.1mol CO�����ܾݴ��ж�ƽ��״̬���ʴ���
C���������ƽ�����������䣬˵�����淴Ӧ������ȣ���Ӧ�ﵽƽ��״̬������ȷ��
D������������䣬����������������䣬���ܾݴ��ж�ƽ��״̬���ʴ���
E��v����CO����v����H2��=1��2�����淴Ӧ������ȣ�˵���ﵽƽ��״̬������ȷ��
��ѡCE��
���CO��ȫ��Ӧ����Ӧ��������������ʵ���Ϊ2mol��Ϊ��Ӧǰ��50%�����Բ����ܴﵽ40%��
�ʴ�Ϊ��0.15 mol/��L��min����CE�����ܣ���Ϊ�÷�ӦΪ���淴Ӧ����CO��ȫ��Ӧʱ��ѹǿΪ��Ӧǰ��50%����˲����ܴﵽ40%��
��3���״����ǻ�����ԭ�ӱ�������ȡ�����ɼ״��ƣ�Ϊ���ӻ��������ʽΪNa+[ ]-���ʴ�Ϊ��Na+[
]-���ʴ�Ϊ��Na+[ ]-��
]-��
��4�������ϼ״�ʧ���Ӻ����������ӷ�Ӧ����̼������Ӻ�ˮ���缫��ӦʽΪCH3OH-6e-+8OH-=CO32-+6H2O���ʴ�Ϊ��CH3OH-6e-+8OH-=CO32-+6H2O��
���� ���⿼����ۺϣ��漰�缫��Ӧʽ����д����ѧƽ��״̬�жϡ�����ʽ����д��֪ʶ�㣬�ѵ��ǻ�ѧƽ��״̬�жϡ��缫��Ӧʽ����д��Ҫ��ϵ������Һ�������д�缫��Ӧʽ���״�ѡ���ǣ�2���е�D��

 Сѧ�̲���ȫ���ϵ�д�
Сѧ�̲���ȫ���ϵ�д�| A�� | Q1=Q | B�� | Q1��Q | C�� | 2Q1��Q | D�� | ���ж� |
| A�� | ��������һ�����ڻ�ѧ�� | |
| B�� | ���������Ӽ�ͨ�������������γɵĻ�ѧ���������Ӽ� | |
| C�� | ֻ�н���Ԫ�غͷǽ���Ԫ�ػ���ʱ�����γ����Ӽ� | |
| D�� | ���ӻ������п��ܺ����ۼ������ۻ������в������Ӽ� |
| A�� | 2H2��g��+O2��g��=2H2O��l������H=Q1 2H2��g��+O2��g��=2H2O��g����H=Q2 | |
| B�� | S��g��+O2��g��=SO2��g������H=Q1 S��s��+O2��g��=SO2��g����H=Q2 | |
| C�� | C��s��+0.5O2��g��=CO��g������H=Q1 C��s��+O2��g��=CO2��g������H=Q2 | |
| D�� | H2��g��+Cl2��g��=2HCl��g������H=Q1 0.5H2��g��+0.5 Cl2��g��=HCl��g������H=Q2 |
| A�� | Li��C��Oԭ�������������������� | B�� | P��S��ClԪ����������ϼ��������� | ||
| C�� | N��O��Fԭ�Ӱ뾶�������� | D�� | Li��Na��K�Ľ�����������ǿ |
| ��� | ��ʵ | ���� |
| A | �ס��������л��������ͬ��Է��������Ͳ�ͬ�ṹ | ����һ����ͬ���칹�� |
| B | ������ͬ�ļס�����������ȫȼ��ʱ����������ͬ��ˮ | �ס������ַ���һ����ͬ���칹�� |
| C | ��������ﰺ�����ȶ������飩������ͬ���칹�� | �������Ϊ�������幹�� |
| D | ��C2H5Br��NaOH����Һ���Ⱥ������ֱ��ͨ������KMnO4��Һ���Ϻ�ɫ��ȥ | ʹKMnO4��ɫ��һ����C2H4 |
| A�� | A | B�� | B | C�� | C | D�� | D |
| �� ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
| 2 | �� | �� | ||||||
| 3 | �� | �� | �� | �� | �� | |||
| 4 | �� | �� |
��2����ЩԪ�ص�����������Ӧ��ˮ�����У�������ǿ�Ļ�����ķ���ʽ��HClO4��������ǿ�Ļ�����ĵ���ʽ
 �����γ��������������Ԫ����Al��
�����γ��������������Ԫ����Al����3���١��ڡ�������Ԫ�ص�ԭ�Ӱ뾶�ɴ�С��˳������ΪK��Na��Mg��
��4����Ԫ�ص��⻯����H2O�����⻯���ڳ�������ڷ�����Ӧ�Ļ�ѧ����ʽΪ2K+2H2O=2KOH+H2����������Һ��pH�� 7��
��5���õ���ʽ��ʾ�ٺ͢�Ԫ���γɻ�����Ĺ���
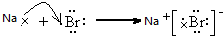 ��
�� 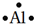
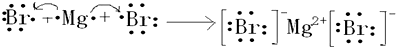
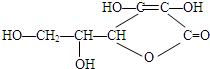 �л�������Ļ�ѧ���ʱ����Ͼ��Ƿ��ӽṹ�����������ŵ����ʣ�
�л�������Ļ�ѧ���ʱ����Ͼ��Ƿ��ӽṹ�����������ŵ����ʣ� ��
��