题目内容
7.在标准状况下,7.84升甲烷完全燃烧后生成二氧化碳和液态水,同时放出311.4kJ的热量.则甲烷燃烧的热化学方程式是( )| A. | CH4+2O2→CO2+2H2O+311.4kJ | B. | CH4(g)+2O2(g)→CO2(g)+2H2O(l)+311.4kJ | ||
| C. | CH4(g)+2O2(g)→CO2(g)+2H2O(l)+889.7kJ | D. | CH4(g)+2O2(g)→CO2(g)+2H2O(g)+889.7kJ |
分析 根据n=$\frac{V}{{V}_{m}}$计算出甲烷的物质的量,然后计算出1mol甲烷完全燃烧放出热量,最后根据热化学方程式的书写原则写出甲烷燃烧的热化学方程式.
解答 解:标准状况下7.84L甲烷的物质的量为:$\frac{7.84L}{22.4L/mol}$=0.35mol,则1mol甲烷完全燃烧放出的热量为:311.4kJ×$\frac{1mol}{0.35mol}$=889.7kJ,
所以甲烷燃烧的热化学方程式为:CH4(g)+2O2(g)→CO2(g)+2H2O(l)+889.7kJ,
故选C.
点评 本题考查了热化学方程式的书写,题目难度不大,明确热化学方程式的书写原则为解答关键,试题侧重基础知识的考查,培养了学生的灵活应用能力.

练习册系列答案
相关题目
17.下列有关阿佛加德罗常数(NA)的说法错误的是( )
| A. | 32g O2所含的原子数目为NA | |
| B. | 0.5mol H2O含有的原子数目为1.5NA | |
| C. | 常温常压下,4.4g CO2 与N2O混合气体中含有的原子总数为0.3NA | |
| D. | 0.5NA个氯气分子的物质的量是0.5mol |
15.向0.1mol•L-1 CH3COOH溶液中加入少量CH3COONa晶体或加水稀释时,都会引起( )
| A. | 溶液的pH增大 | B. | CH3COOH的电离程度增大 | ||
| C. | 溶液的导电能力减小 | D. | 溶液中n(H+)减小 |
2.下列措施中能促进水的电离的是( )
| A. | 加热 | B. | 加入水 | C. | 加入碳酸钠 | D. | 滴加醋酸 |
12.下列叙述中正确的是( )
| A. | N、O、P元素的非金属性依次减弱 | |
| B. | Na、Mg、Al元素最高化合价依次升高 | |
| C. | Na、Li、K原子的电子层数依次增多 | |
| D. | P、Cl、S元素最高价氧化物对应的水化物酸性依次增强 |
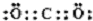 ,属于两性氢氧化物的电离方程式Al3++3OH-?Al(OH)3 ?H++AlO2-+H2O.
,属于两性氢氧化物的电离方程式Al3++3OH-?Al(OH)3 ?H++AlO2-+H2O.