题目内容
2.下列措施中能促进水的电离的是( )| A. | 加热 | B. | 加入水 | C. | 加入碳酸钠 | D. | 滴加醋酸 |
分析 水为弱电解质,能够电解出氢离子和氢氧根离子,在溶液中存在电离平衡;加入酸溶液和碱溶液能够抑制水的电离,加入能够水解的盐促进了水的电离,据此进行判断.
解答 解:A、水是弱电解质,电离吸热,故加热能促进水的电离,故A正确;
B、由于水为纯液体,故再加入水,水的浓度不变,电离平衡不移动,故B错误;
C、碳酸钠为强碱弱酸盐,碳酸根在溶液中会水解,对水的电离有促进作用,故C正确;
D、加入醋酸,醋酸电离出的氢离子对水的电离有抑制作用,故D错误;
故选AC.
点评 本题考查了水的电离及其影响因素,题目难度不大,注意掌握水的电离及影响,明确酸碱溶液抑制水的电离,含有弱酸根或者弱碱根离子的盐能够促进水的电离.

练习册系列答案
相关题目
12.下列有关化学用语表示正确的是( )
| A. | 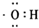 为羟基的电子式,也是氢氧根离子的电子式 为羟基的电子式,也是氢氧根离子的电子式 | |
| B. | S2-的结构示意图: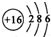 | |
| C. | 甲烷分子的比例模型是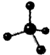 | |
| D. | 中子数为10的氧原子:18O |
13.如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此下列说法正确的是( )


| A. | 该试剂的物质的量浓度为9.2 mol/L | |
| B. | 该硫酸50 mL若用5 mol/L的氢氧化钠中和,需要该氢氧化钠溶液100毫升 | |
| C. | 该硫酸与等体积的水混合所得溶液的质量分数等于49% | |
| D. | 配制200 mL 4.6 mol/L的稀硫酸需取该硫酸50 mL |
10.质量相等的下列物质中,所含原子数最少的是( )
| A. | H2O | B. | NH3 | C. | CH4 | D. | H3PO4 |
17.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 将1mol明矾晶体完全溶于水制成胶体,其中所含胶体粒子数目为NA | |
| B. | 在反应KIO3+6HI=KI+3I2+3H2O中,每生成3molI2转移的电子数为5NA | |
| C. | 0.1 mol•Lˉ1 CaCl2溶液中含有Clˉ离子的数目为0.2NA | |
| D. | 136g熔融的KHSO4中含有2NA个阳离子 |
7.在标准状况下,7.84升甲烷完全燃烧后生成二氧化碳和液态水,同时放出311.4kJ的热量.则甲烷燃烧的热化学方程式是( )
| A. | CH4+2O2→CO2+2H2O+311.4kJ | B. | CH4(g)+2O2(g)→CO2(g)+2H2O(l)+311.4kJ | ||
| C. | CH4(g)+2O2(g)→CO2(g)+2H2O(l)+889.7kJ | D. | CH4(g)+2O2(g)→CO2(g)+2H2O(g)+889.7kJ |
14.人类生活离不开化学,以下是补铁剂和胃药的两张标签的部分信息.
Ⅰ、根据“硫酸亚铁片”标签回答问题
(1)硫酸亚铁片中糖衣的作用是隔绝空气,防止FeSO4被空气氧化.
(2)检验硫酸亚铁片是否被氧化的试剂是KSCN溶液.
(3)硫酸盐中检验SO42-的离子反应方程式是Ba2++SO42-→BaSO4↓.
(4)鉴别中,“加稀盐酸1滴”的作用是B(选填序号)
A.防止亚铁离子被氧化 B、抑制亚铁离子水解
Ⅱ、根据“氢氧化铝片”标签回答问题
(1)能缓解胃酸过多的成分是MgCO3、Al(OH)3.
(2)写出氢氧化铝中和胃酸反应的离子方程式Al(OH)3+3H+=Al3++3H2O.
(3)明矾石是制取钾肥和氢氧化铝的重要原料,明矾石的组成和明矾相似,此外还含有氧化铝和少量氧化铁杂质.具体实验步骤如图所示:
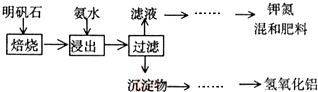
根据上述图示,完成下列填空:
①制备过程中多次用到过滤操作,在实验室中该操作所需的玻璃仪器除了烧杯、漏斗外,还需玻璃棒.
②明矾石焙烧后用稀氨水浸出.配制500mL稀氨水(每升含有39.20g氨)需要取浓氨水(每升含有250.28g氨)78mL,用规格为100mL量筒量取(可供选择的量筒有10mL、50mL、100mL、200mL四种规格).
③写出沉淀物中所有物质的化学式Al(OH)3、Al2O3、Fe2O3.
④为测定明矾石中铝元素的含量,称取m g 明矾石样品按上述流程制得氢氧化铝n g(假设整个流程中既无铝元素损失,也无铝元素的引入),则该明矾石样品中铝元素的质量分数为:$\frac{27n}{78m}$×100% (用含m、n的代数式表示).
| 硫酸亚铁片 英文名:Ferrous Sulfate Tablets 本品含硫酸亚铁(FeSO4•7H2O)应为标示量的95.0%~110.0% | 氢氧化铝片 英文名:Aluminium Hydroxide Tablets |
| 【主要成分】糖衣、碳酸镁、氢氧化铝、淀粉 | |
| 【性状】本品为糖衣,除去糖衣后显淡绿色 | 【适应症】能缓解胃酸过多 |
| 【鉴别】取本品,除去糖衣,称取适量(约相当于硫酸亚铁片0.2g),加稀盐酸1滴与水20ml,振摇使硫酸亚铁溶解,过滤,滤液进行亚铁盐与硫酸盐的鉴别反应 | 【用法用量】成人:口服,一次0.6~0.9g(一次2~3片),一日3次,餐前1小时服用 |
| 【详细用法】详见说明书 |
(1)硫酸亚铁片中糖衣的作用是隔绝空气,防止FeSO4被空气氧化.
(2)检验硫酸亚铁片是否被氧化的试剂是KSCN溶液.
(3)硫酸盐中检验SO42-的离子反应方程式是Ba2++SO42-→BaSO4↓.
(4)鉴别中,“加稀盐酸1滴”的作用是B(选填序号)
A.防止亚铁离子被氧化 B、抑制亚铁离子水解
Ⅱ、根据“氢氧化铝片”标签回答问题
(1)能缓解胃酸过多的成分是MgCO3、Al(OH)3.
(2)写出氢氧化铝中和胃酸反应的离子方程式Al(OH)3+3H+=Al3++3H2O.
(3)明矾石是制取钾肥和氢氧化铝的重要原料,明矾石的组成和明矾相似,此外还含有氧化铝和少量氧化铁杂质.具体实验步骤如图所示:

根据上述图示,完成下列填空:
①制备过程中多次用到过滤操作,在实验室中该操作所需的玻璃仪器除了烧杯、漏斗外,还需玻璃棒.
②明矾石焙烧后用稀氨水浸出.配制500mL稀氨水(每升含有39.20g氨)需要取浓氨水(每升含有250.28g氨)78mL,用规格为100mL量筒量取(可供选择的量筒有10mL、50mL、100mL、200mL四种规格).
③写出沉淀物中所有物质的化学式Al(OH)3、Al2O3、Fe2O3.
④为测定明矾石中铝元素的含量,称取m g 明矾石样品按上述流程制得氢氧化铝n g(假设整个流程中既无铝元素损失,也无铝元素的引入),则该明矾石样品中铝元素的质量分数为:$\frac{27n}{78m}$×100% (用含m、n的代数式表示).
11.与新能源相关的核反应是21H+31H→42He+10n,关于这个核反应的下列说法中正确的是( )
| A. | 聚变反应 释放核能 | B. | 聚变反应 吸收核能 | ||
| C. | 裂变反应 释放核能 | D. | 裂变反应 吸收核能 |