题目内容
6.马利亚纳海沟是世界上最深的海沟,深11km,科学家进行考察时发现海沟深处有鱼虾,却没有绿色植物其原因是( )| A. | 没有阳光 | B. | 温度太低 | C. | 压强太大 | D. | 缺少CO2和O2 |
分析 光在海水中的穿透性由浅到深,越来越弱,海沟中没有阳光,植物无法进行光化作用.
解答 解:光在海水中的穿透性由浅到深,越来越弱,海沟中没有阳光,绿色植物的光化作用需要阳光,没有阳光,植物无法进行光化作用,所以海沟深处绿色植物,
故选A.
点评 本题考查了植物光化作用的条件,侧重于考查学生的分析能力和对基础知识的应用能力,题目难度不大.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案
相关题目
3.X、Y、Z、W为原子序数依次增大的四种短周期主族元素,且最外层电子数之和为20.X与Y、Z位于相邻周期,Z元素原子最外层电子数既是X元素原子内层电子数的3倍,又是Y元素原子最外层电子数的2倍.下列说法正确的是( )
| A. | 原子半径:Z>Y>X | |
| B. | 最高价氧化物对应水化物的酸性:Z>X | |
| C. | 最简单氢化物的稳定性:W<Z<X | |
| D. | Y的氧化物不属于两性氧化物 |
20.下列物质的应用或现象解释错误的是( )
| A. | 废旧电池必须回收,主要目的是回收其中的金属 | |
| B. | “从沙滩到用户”,计算机芯片的材料是指单质硅 | |
| C. | 利用风能,太阳能等清洁能源代替化石燃料,可减少环境污染 | |
| D. | “光化学烟雾”,“硝酸型酸雨”的形成都与氮氧化物有关 |
1.将等物质的量的氧化钠和过氧化钠分别放入等质量的过量的水中,得到溶液的质量分别为a g和b g,(设反应中水分不损失)则a和b的关系为( )
| A. | a<b | B. | a>b | C. | a=b | D. | 无法确定 |
11.下列溶液中Cl-的物质的量浓度最大的是( )
| A. | 200mL 2mol/L MgCl2溶液 | B. | 1000mL 2.5mol/L NaCl溶液 | ||
| C. | 250mL 1mol/L AlCl3溶液 | D. | 300mL 5mol/L KCl溶液 |
18.下列分子中含有“手性碳原子”的是( )
| A. | CBr2F2 | B. | CH3CH2OH | C. | CH3CH2CH3 | D. | CH3CH(OH)COOH |
15.(1)25℃,吸收液Na2SO3溶液在吸收SO2的过程中,pH随n(SO32-):n(HSO3-)变化关系如下表:
①当吸收液呈中性时,溶液中离子浓度关系正确的是:AB(选填字母)
A.c(Na+)=2c(SO32-)+c(HSO3-)
B.c(Na+)>c(HSO3-)>c(SO32-)>c(H+)=c(OH-)
C.c(Na+)+c(H+)=c(SO32-)+c(HSO3-)+c(OH-)
②当吸收液的pH降至约为6时,需送至电解槽再生.再生示意图如下:
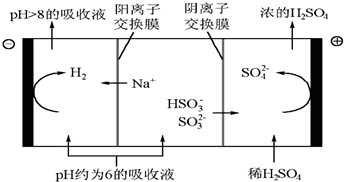
请写出HSO3-在阳极放电的电极反应式是HSO3-+H2O-2e-=SO42-+3H+.
(2)已知:CH4(g)+2O2(g)=CO2 (g)+2H2O (l)△H=-Q1 kJ/mol
2H2(g)+O2(g)=2H2 O (g)△H=-Q2 kJ/mol
2H2(g)+O2(g)=2H2 O (l)△H=-Q3 kJ/mol,
常温下,取体积比4:1的甲烷和氢气的混合气体11.2L(标况),经完全燃烧恢复常温,放出的热为0.4Q1+0.05Q3.
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 1:91 |
| pH | 8.2 | 7.2 | 6.2 |
A.c(Na+)=2c(SO32-)+c(HSO3-)
B.c(Na+)>c(HSO3-)>c(SO32-)>c(H+)=c(OH-)
C.c(Na+)+c(H+)=c(SO32-)+c(HSO3-)+c(OH-)
②当吸收液的pH降至约为6时,需送至电解槽再生.再生示意图如下:

请写出HSO3-在阳极放电的电极反应式是HSO3-+H2O-2e-=SO42-+3H+.
(2)已知:CH4(g)+2O2(g)=CO2 (g)+2H2O (l)△H=-Q1 kJ/mol
2H2(g)+O2(g)=2H2 O (g)△H=-Q2 kJ/mol
2H2(g)+O2(g)=2H2 O (l)△H=-Q3 kJ/mol,
常温下,取体积比4:1的甲烷和氢气的混合气体11.2L(标况),经完全燃烧恢复常温,放出的热为0.4Q1+0.05Q3.