题目内容
由Na2SO4和NaNO3组成的混合物88g溶于水配制成1L溶液,此溶液中Na+的浓度为1.2mol/L,则原混合物中NaNO3的质量为( )
| A、17g | B、34g |
| C、25.5g | D、51g |
考点:溶液中溶质的质量分数及相关计算
专题:计算题
分析:制成1L溶液,此溶液中Na+的浓度为1.2mol/L,可以据此计算溶液中钠离子的总物质的量,根据质量和物质的量之间的关系计算混合物中NaNO3的质量.
解答:
解:制成1L溶液,此溶液中Na+的浓度为1.2mol/L,则溶液中钠离子的总物质的量n=cV=×1L=1.2mol,设:原混合物中NaNO3的物质的量为x,Na2SO4的物质的量是y,则x+2y=1.2,142y+85x=88,解得x=0.2,y=0.5,则硝酸钠的质量m=0.2mol×85g/mol=17g.
故选A.
故选A.
点评:本题考查学生物质的质量的计算m=nM的应用,注意知识的归纳和整理是关键,难度不大.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
用NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A、0.5mol O2所含氧元素数为NA |
| B、0.2mol H2O所含的H原子数为0.2NA |
| C、0.1mol CH4所含电子数为NA |
| D、46克NO2和N2O4的混合物含有的分子数为NA |
 某物质的晶体中含Ti、O、Ca三种元素,其晶胞排列方式如图所示,晶体中Ti、O、Ca的中原子个数之比为( )
某物质的晶体中含Ti、O、Ca三种元素,其晶胞排列方式如图所示,晶体中Ti、O、Ca的中原子个数之比为( )| A、1:3:1 |
| B、2:3:1 |
| C、2:2:1 |
| D、1:3:3 |
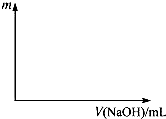 将等物质的量的两种氧化物溶于100mL硫酸,而后逐滴加入1.00mol?L-1的NaOH溶液.当加入的NaOH的体积V1=50mL时,开始有沉淀析出,且沉淀量随NaOH加入量逐渐增加;当NaOH的体积V2=650mL 时,沉淀量达最大值,继续滴加NaOH时,沉淀量逐渐减小;当V3≥750mL时,沉淀量不再改变.
将等物质的量的两种氧化物溶于100mL硫酸,而后逐滴加入1.00mol?L-1的NaOH溶液.当加入的NaOH的体积V1=50mL时,开始有沉淀析出,且沉淀量随NaOH加入量逐渐增加;当NaOH的体积V2=650mL 时,沉淀量达最大值,继续滴加NaOH时,沉淀量逐渐减小;当V3≥750mL时,沉淀量不再改变.