题目内容
8.已知常温下1g丙烷(C3H8)完全燃烧放热50.4kJ,则反应的热化学方程式为:C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)△H=-2217.6kJ/mol.分析 1g丙烷(C3H8)完全燃烧放热50.4kJ,则1molC3H8完全燃烧放热为50.4kJ×44=2217.6kJ,结合物质的状态、焓变书写热化学方程式.
解答 解:1g丙烷(C3H8)完全燃烧放热50.4kJ,则1molC3H8完全燃烧放热为50.4kJ×44=2217.6kJ,可知丙烷燃烧的热化学方程式为C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)△H=-2217.6kJ/mol,
故答案为:C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)△H=-2217.6kJ/mol.
点评 本题考查热化学方程式的书写,为高频考点,把握反应中能量变化、焓变为解答的关键,侧重分析与应用能力的考查,注意物质的量与热量成正比,题目难度不大.

练习册系列答案
相关题目
19.下列物质属于电解质的是( )
| A. | 次氯酸 | B. | 细铁丝 | C. | 氯水 | D. | 干冰 |
16.对碱性锌锰电池的判断正确的是( )
| A. | 锌为负极,二氧化锰为正极 | |
| B. | 锌为正极,二氧化锰为负极 | |
| C. | 工作时电子由二氧化锰经外电路流向锌极 | |
| D. | 锌电极发生还原反应,二氧化锰发生氧化反应 |
3.CuCl是白色粉末,不溶于水、乙醇及稀硫酸,熔点422℃,沸点1366℃,在空气中迅速被氧化成绿色,常用作有机合成工业中的催化剂,并用于颜料、防腐等工业.工业上由废铜料(含Fe、Al及其化合物、SiO2杂质),生产CuCl的工艺流程如图:
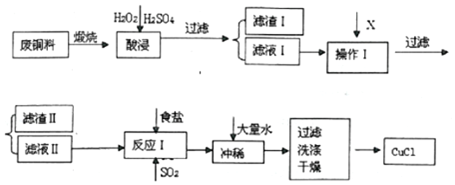
已知:CuCl溶于NaCl的浓溶液可生成CuCl2-,CuCl2-的溶液用水稀释后可生成CuCl沉淀.
(1)酸浸液中加入足量H2O2的主要目的是将Fe2+完全氧化为Fe3+,便于转化为Fe(OH)3沉淀除去.
(2)滤渣I的主要成分是SiO2.
(3)操作I调节溶液的pH范围为4.7≤pH≤5.6,加入的物质X可以是ABCD.
A.CuO B.Cu(OH)2 C.NaOH溶液 D.Cu2(OH)2CO E.Cu
(4)往滤液 II中加入食盐并通入SO2可生成CuCl2-,请写出反应的离子方程式2H2O+2Cu2++SO2+4Cl-=2CuCl2-+SO42-+4H+.
(5)过滤得到CuCl沉淀,用无水乙醇洗涤沉淀,在真空干燥机内于70℃干燥2小时,冷却,密封包装即得产品.于70℃真空干燥的目的是:加快乙醇和水的蒸发,防止CuCl被空气氧化.
(6)氯化亚铜的定量分析:
①称取样品0.25g置于预先放入玻璃珠50粒和10mL过量的FeCl3溶液250mL锥形瓶中,不断摇动:玻璃珠的作用是加速样品的溶解.
②待样品溶解后,加水50mL,并加入邻菲罗啉指示剂2滴:
③立即用0.10mol•L-1硫酸铈标准溶液滴至终点:同时做空白实验一次.
己知:上述过程发生的反应①CuCl+FeCl3═CuCl2+FeCl2③Fe2++Ce4+═Fe3++Ce3+
如此再重复二次测得:
④数据处理:计算得CuCl的纯度为95.52%.(平行实验结果相差不能超过0.3%)
(说明:空白实验是在不加样品的情况下,用测定样品相同的方法、步骤进行定量分析,把所得结果作为空白值,从样品的分析结果中扣除.这样可以消除由于试剂不纯或试剂干扰等所造成的系统误差.)

| 物质 | 开始沉淀pH | 沉淀完全pH |
| Fe(OH)3 | 2.2 | 3.2 |
| Cu(OH)2 | 5.6 | 6.7 |
| Al(OH)3 | 3.7 | 4.7 |
| Fe(OH)2 | 7.6 | 9.6 |
(1)酸浸液中加入足量H2O2的主要目的是将Fe2+完全氧化为Fe3+,便于转化为Fe(OH)3沉淀除去.
(2)滤渣I的主要成分是SiO2.
(3)操作I调节溶液的pH范围为4.7≤pH≤5.6,加入的物质X可以是ABCD.
A.CuO B.Cu(OH)2 C.NaOH溶液 D.Cu2(OH)2CO E.Cu
(4)往滤液 II中加入食盐并通入SO2可生成CuCl2-,请写出反应的离子方程式2H2O+2Cu2++SO2+4Cl-=2CuCl2-+SO42-+4H+.
(5)过滤得到CuCl沉淀,用无水乙醇洗涤沉淀,在真空干燥机内于70℃干燥2小时,冷却,密封包装即得产品.于70℃真空干燥的目的是:加快乙醇和水的蒸发,防止CuCl被空气氧化.
(6)氯化亚铜的定量分析:
①称取样品0.25g置于预先放入玻璃珠50粒和10mL过量的FeCl3溶液250mL锥形瓶中,不断摇动:玻璃珠的作用是加速样品的溶解.
②待样品溶解后,加水50mL,并加入邻菲罗啉指示剂2滴:
③立即用0.10mol•L-1硫酸铈标准溶液滴至终点:同时做空白实验一次.
己知:上述过程发生的反应①CuCl+FeCl3═CuCl2+FeCl2③Fe2++Ce4+═Fe3++Ce3+
如此再重复二次测得:
| 1 | 2 | 3 | |
| 空白实验消耗硫酸铈标准溶液的体积(mL) | 0.75 | 0.50 | 0.80 |
| 0.25g样品消耗硫酸铈标准溶液的体积(mL) | 24.75 | 24.85 | 24.80 |
(说明:空白实验是在不加样品的情况下,用测定样品相同的方法、步骤进行定量分析,把所得结果作为空白值,从样品的分析结果中扣除.这样可以消除由于试剂不纯或试剂干扰等所造成的系统误差.)
13.根据实验室测定硫酸铜晶体(CuSO4•xH2O)结晶水含量的实验,填写下列空白.
(1)某学生实验后得到表数据:
测得平均结晶水x=4.1(保留2位小数),相对误差=18%(保留2位小数).
(2)从下列选项中选出该学生产生误差的原因可能是(填写字母)CD.
A.加热前称量时容器未完全干燥
B.加热过程中晶体有少量溅失
C.加热后容器未放入干燥器中冷却
D.硫酸铜晶体中含有不分解失重的杂质.
(1)某学生实验后得到表数据:
| 实验 序号 | 加热前的质量 | 加热后的质量 | 失水质量 | 结晶水的值 | |
| m0(容器) | m1(容器+晶体) | m2(容器+无水硫酸铜) | |||
| 1 | 35.503g | 35.685g | 35.620g | ①0.065 | ②4.9 |
| 2 | 35.503g | 35.663g | 35.606g | ③0.057 | ④3.2 |
(2)从下列选项中选出该学生产生误差的原因可能是(填写字母)CD.
A.加热前称量时容器未完全干燥
B.加热过程中晶体有少量溅失
C.加热后容器未放入干燥器中冷却
D.硫酸铜晶体中含有不分解失重的杂质.
20.对下列现象或事实的解释不正确的是( )
| 选项 | 现象或事实 | 解释 |
| A | 铝箔在酒精灯上加热,熔化后的液态铝不滴落 | 高熔点的氧化铝薄膜兜在铝的外面,阻止了液态铝滴落 |
| B | 铁放在冷的浓硝酸中不溶解,无红棕色气体生成 | 铁遇浓硝酸钝化,表面形成致密的氧化膜,阻止内部铁继续与硝酸反应 |
| C | 漂白粉在空气中久置变质 | 漂白粉中的CaCl2与空气中的CO2反应生成CaCO3 |
| D | 将新制氯水滴到蓝色石蕊试纸上,试纸先变红后褪色 | 新制氯水中的H+使石蕊试纸先变红,HClO的强氧化性使石蕊试纸褪色 |
| A. | A | B. | B | C. | C | D. | D |
5.铝制品具有较强的抗腐蚀性,主要是因为( )
| A. | 铝的化学性质稳定 | |
| B. | 铝在常温时与氧气不反应 | |
| C. | 铝具有金属性,也具有非金属性 | |
| D. | 铝与氧气反应生成一层致密的氧化物薄膜 |
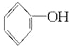 +2Na→2
+2Na→2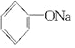 +H2↑
+H2↑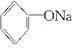 +H2O.
+H2O.