题目内容
5.铝制品具有较强的抗腐蚀性,主要是因为( )| A. | 铝的化学性质稳定 | |
| B. | 铝在常温时与氧气不反应 | |
| C. | 铝具有金属性,也具有非金属性 | |
| D. | 铝与氧气反应生成一层致密的氧化物薄膜 |
分析 铝属于亲氧元素,极易被空气中氧气氧化生成一层致密的氧化物薄膜而阻止进一步被氧化,据此分析解答.
解答 解:A.铝是活泼金属,化学性质活泼,故A错误;
B.铝被氧气氧化生成氧化铝,而不是不反应,故B错误;
C.铝具有金属性,不具有非金属性,故C错误;
D.铝被氧气氧化生成氧化铝,氧化铝是致密的氧化物,能阻止铝进一步被氧化,故D正确;
故选D.
点评 本题以铝的抗腐蚀性能为载体考查了铝的性质,铝是中学阶段学习的唯一一个能和酸、强碱反应的金属,常常在推断题中考查,明确铝比铁活泼,但铝比铁抗腐蚀性强的原因,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.用NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4 L乙烯含有的共用电子对数为5NA | |
| B. | 8.0gCu2S和CuO的混合物中含有的铜原子数为0.1NA | |
| C. | 电解饱和食盐水时,阳极生成22.4L气体时,转移的电子数为2NA | |
| D. | 室温下向1L pH=1的醋酸溶液中加水,所得溶液中H+数目小于0.1NA |
6.短周期元素W、X、Y、Z在元素周期表中的相对位置如表所示,这四种元素的原子最外层电子数之和为21.下列说法不正确的是( )
| W | |||
| X | Y | Z |
| A. | 原子半径大小:X>Y>Z | |
| B. | W、Y两种元素都能与氧元素形成化合物WO2、YO2 | |
| C. | 最高价氧化物对应水化物的酸性:W>Y>Z | |
| D. | W元素的单质能从X的氧化物中置换出X单质 |
17.实验室制取氯气反应为:MnO2+4HCl(浓) $\frac{\underline{\;△\;}}{\;}$MnCl2+Cl2↑+2H2O,现在用下列两种方法制取氯气:①用含HCl 146g的浓盐酸与足量的MnO2 反应;②用87g MnO2与足量浓盐酸反应.所得的氯气( )
| A. | ①比②多 | B. | ②比①多 | C. | 一样多 | D. | 无法比较 |
15.“酸雨”的形成主要是由于是( )
| A. | 煤燃烧时产生大量CO2 | B. | 煤不完全燃烧产生大量CO | ||
| C. | 煤燃烧时产生大量SO2 | D. | 工业生产中排放大量烟尘 |
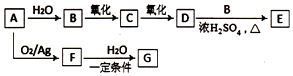 A是一种重要的化工原料,C、F的分子式都为C2H4O,F是没有不饱和键的环状有机物,G的分子式为C2H6O2,G中含有两个相同的官能团,转化关系如图:
A是一种重要的化工原料,C、F的分子式都为C2H4O,F是没有不饱和键的环状有机物,G的分子式为C2H6O2,G中含有两个相同的官能团,转化关系如图: .
.