��Ŀ����
��14�֣���һ�������£���������������������·�Ӧ:2SO2(g)+ O2 (g)  2SO3(g) ��H< 0����������֪SO3�۵�16.83�棬�е�44.8�档
2SO3(g) ��H< 0����������֪SO3�۵�16.83�棬�е�44.8�档
��1��600��ʱ����һ�ܱ������У������������������ϣ���Ӧ������SO2��O2��SO3���ʵ����仯��ͼ��
�ٸ÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽ K=
�ڸ÷�Ӧ���Է����е�ԭ���� ��
�۾�ͼ�жϣ��÷�Ӧ����ƽ��״̬��ʱ���� ��
�ܾ�ͼ�жϣ���Ӧ������20 minʱ�����߷����仯��ԭ���� �������ֱ����
��2��ij��ѧ�о�ѧϰС������ͼ��װ����װ�����һ��ʵ�飬�ԲⶨSO2ת��ΪSO3��ת���ʣ�����������˳����a��h��i��b��c��f��g��d��e��
��Ϊ���SO2��ת���ʣ�ʵ��ʱ����Ũ��������ȴ������Ⱥ�˳���� ��
���ڢ��ô�������ƿʱSO2��ת���ʻ� �����������䡱��С����
����n mol Na2SO3��ĩ������Ũ������д�ʵ�飬����Ӧ����ʱ������ͨ��O2һ��ʱ��Ƶâ����� m g����ʵ����SO2��ת����Ϊ ��
��1����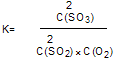 �ڸ÷�Ӧ�Ƿ��ȷ�Ӧ
�ڸ÷�Ӧ�Ƿ��ȷ�Ӧ
��15��20 25��30 ������������Ũ�ȣ������ʵ�����
��2�����ȼ��Ȣ��� �ڼ�С ��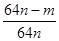 ��100%
��100%
����

 ���������к�ƻ���ף�ƻ������һ����ƻ�����Ͷ��ɵľ��нⶾ����֬�����ʺ�ֹк�����õı���ʳƷ��ƻ���ᣨ��-�ǻ������ᣩ���������ϵ���Ҫ�������ʣ���ṹ��ͼ��ʾ���������˵����ȷ���ǣ�������
���������к�ƻ���ף�ƻ������һ����ƻ�����Ͷ��ɵľ��нⶾ����֬�����ʺ�ֹк�����õı���ʳƷ��ƻ���ᣨ��-�ǻ������ᣩ���������ϵ���Ҫ�������ʣ���ṹ��ͼ��ʾ���������˵����ȷ���ǣ�������| A��ƻ������һ���������ܷ�����ȥ��Ӧ | B��ƻ������һ���������ܴ���������ȩ | C��ƻ������һ���������ܷ����Ӿ۷�Ӧ���ɸ߷��ӻ����� | D��1 molƻ������NaHCO3��Һ��Ӧ�������3 mol NaHCO3 |




