题目内容
标准状况下,将aLH2和Cl2的混合气体点燃,充分反应后,将混合气体通入含bmolNaOH的热溶液中,气体恰好被完全吸收,NaOH无剩余,测得反应后溶液中含Cl-、ClO-、ClO-3,且三者的物质的量之比为8:1:1,则原混合气体中H2的物质的量为
- A.
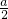 mol
mol - B.(
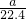 -b)mol
-b)mol - C.(
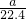 -
-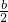 )mol
)mol - D.
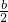 mol
mol
C
分析:方法一:将混合气体通入含bmolNaOH的热溶液中,气体恰好被完全吸收,NaOH无剩余,测得反应后溶液中含Cl-、ClO-、ClO-3,根据电荷守恒可知,溶液中n(Na+)=n(Cl-)+n(ClO-)+n(ClO-3),根据氯元素守恒,计算aLH2和Cl2的混合气体中氯气的物质的量,aLH2和Cl2的混合气体总的物质的量减去氯气的物质的量即为氢气的物质的量.
方法二:将混合气体通入含bmolNaOH的热溶液中,气体恰好被完全吸收,NaOH无剩余,测得反应后溶液中含Cl-、ClO-、ClO-3,根据电荷守恒可知,溶液中n(Na+)=n(Cl-)+n(ClO-)+n(ClO-3),溶液中Cl-、ClO-、ClO-3三者的物质的量之比为8:1:1,据此计算各离子物质的量,根据电子转移守恒,计算氯气发生氧化还原反应生成的氯离子的物质的量,溶液中Cl-来源于氯化氢及氯气与氢氧化钠的反应,计算反应后混合气体中氯化氢的物质的量,根据氢元素守恒计算氢气的物质的量.
解答:方法一:混合气体通入含bmolNaOH的热溶液中,气体恰好被完全吸收,NaOH无剩余,测得反应后溶液中含Cl-、ClO-、ClO-3,根据电荷守恒可知,溶液中n(Na+)=n(Cl-)+n(ClO-)+n(ClO-3),
根据氯元素守恒可知,aLH2和Cl2的混合气体中n(Cl2)= [n(Cl-)+n(ClO-)+n(ClO-3)]=
[n(Cl-)+n(ClO-)+n(ClO-3)]= n(Na+)=
n(Na+)= bmol,所以aLH2和Cl2的混合气体中n(H2)=(
bmol,所以aLH2和Cl2的混合气体中n(H2)=(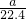 -
-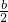 )mol
)mol
方法二:混合气体通入含bmolNaOH的热溶液中,气体恰好被完全吸收,NaOH无剩余,测得反应后溶液中含Cl-、ClO-、ClO-3,根据电荷守恒可知,溶液中n(Na+)=n(Cl-)+n(ClO-)+n(ClO-3),
由于溶液中Cl-、ClO-、ClO-3三者的物质的量之比为8:1:1,所以溶液中n(Cl-)=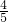 bmol,n(ClO-)=
bmol,n(ClO-)=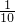 bmol,n(ClO-3)=
bmol,n(ClO-3)=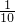 bmol,
bmol,
令氯气与氢氧化钠反应生成的氯离子的物质的量为xmol,根据电子转移守恒有x=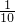 b+
b+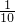 bmol×5=
bmol×5=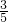 bmol,
bmol,
溶液中Cl-来源于氯化氢及氯气与氢氧化钠的反应,所以氯化氢提供的氯离子为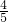 bmol-
bmol-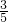 bmol=
bmol= molb,
molb,
即反应后的混合气体中n(HCl)= bmol,根据氢元素守恒可知,n(H2)=
bmol,根据氢元素守恒可知,n(H2)= n(HCl)=
n(HCl)= ×
× molb=0.1bmol,
molb=0.1bmol,
故选:C.
点评:考查氧化还原反应的计算,难度中等,判断溶液中n(Na+)=n(Cl-)+n(ClO-)+n(ClO-3)是解题关键.
分析:方法一:将混合气体通入含bmolNaOH的热溶液中,气体恰好被完全吸收,NaOH无剩余,测得反应后溶液中含Cl-、ClO-、ClO-3,根据电荷守恒可知,溶液中n(Na+)=n(Cl-)+n(ClO-)+n(ClO-3),根据氯元素守恒,计算aLH2和Cl2的混合气体中氯气的物质的量,aLH2和Cl2的混合气体总的物质的量减去氯气的物质的量即为氢气的物质的量.
方法二:将混合气体通入含bmolNaOH的热溶液中,气体恰好被完全吸收,NaOH无剩余,测得反应后溶液中含Cl-、ClO-、ClO-3,根据电荷守恒可知,溶液中n(Na+)=n(Cl-)+n(ClO-)+n(ClO-3),溶液中Cl-、ClO-、ClO-3三者的物质的量之比为8:1:1,据此计算各离子物质的量,根据电子转移守恒,计算氯气发生氧化还原反应生成的氯离子的物质的量,溶液中Cl-来源于氯化氢及氯气与氢氧化钠的反应,计算反应后混合气体中氯化氢的物质的量,根据氢元素守恒计算氢气的物质的量.
解答:方法一:混合气体通入含bmolNaOH的热溶液中,气体恰好被完全吸收,NaOH无剩余,测得反应后溶液中含Cl-、ClO-、ClO-3,根据电荷守恒可知,溶液中n(Na+)=n(Cl-)+n(ClO-)+n(ClO-3),
根据氯元素守恒可知,aLH2和Cl2的混合气体中n(Cl2)=
 [n(Cl-)+n(ClO-)+n(ClO-3)]=
[n(Cl-)+n(ClO-)+n(ClO-3)]= n(Na+)=
n(Na+)= bmol,所以aLH2和Cl2的混合气体中n(H2)=(
bmol,所以aLH2和Cl2的混合气体中n(H2)=(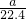 -
-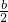 )mol
)mol方法二:混合气体通入含bmolNaOH的热溶液中,气体恰好被完全吸收,NaOH无剩余,测得反应后溶液中含Cl-、ClO-、ClO-3,根据电荷守恒可知,溶液中n(Na+)=n(Cl-)+n(ClO-)+n(ClO-3),
由于溶液中Cl-、ClO-、ClO-3三者的物质的量之比为8:1:1,所以溶液中n(Cl-)=
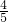 bmol,n(ClO-)=
bmol,n(ClO-)=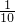 bmol,n(ClO-3)=
bmol,n(ClO-3)=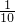 bmol,
bmol,令氯气与氢氧化钠反应生成的氯离子的物质的量为xmol,根据电子转移守恒有x=
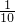 b+
b+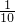 bmol×5=
bmol×5=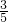 bmol,
bmol,溶液中Cl-来源于氯化氢及氯气与氢氧化钠的反应,所以氯化氢提供的氯离子为
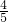 bmol-
bmol-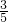 bmol=
bmol= molb,
molb,即反应后的混合气体中n(HCl)=
 bmol,根据氢元素守恒可知,n(H2)=
bmol,根据氢元素守恒可知,n(H2)= n(HCl)=
n(HCl)= ×
× molb=0.1bmol,
molb=0.1bmol,故选:C.
点评:考查氧化还原反应的计算,难度中等,判断溶液中n(Na+)=n(Cl-)+n(ClO-)+n(ClO-3)是解题关键.

练习册系列答案
相关题目
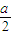 mol
mol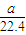 -b)mol
-b)mol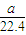 -
-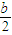 )mol
)mol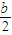 mol
mol