题目内容
下列有关实验操作的说法正确的是( )
| A、SO2通入酸性高锰酸钾溶液中,溶液褪色,说明SO2具有漂白性 | B、用蒸馏水将PH试纸先润湿,可用于检验氨气 | C、可用瓷坩埚熔化各种钠的化合物 | D、某溶液中加Ba(NO3)2溶液,再加入稀盐酸,沉淀不溶解,则原溶液中一定有SO42- |
分析:A.酸性高锰酸钾溶液褪色,体现二氧化硫的还原性;
B.氨气是碱性气体,氨气能使湿润的红色石蕊试纸变蓝;
C.瓷坩埚成分中含二氧化硅,能和氢氧化钠发生反应;
D.根据加入硝酸钡,溶液中存在了硝酸根离子,再加入盐酸时引入氢离子,就相当于存在了硝酸,将亚硫酸根离子氧化为硫酸根离子,与钡离子形成不可溶的硫酸钡沉淀,也可能含有亚硫酸根离子.
B.氨气是碱性气体,氨气能使湿润的红色石蕊试纸变蓝;
C.瓷坩埚成分中含二氧化硅,能和氢氧化钠发生反应;
D.根据加入硝酸钡,溶液中存在了硝酸根离子,再加入盐酸时引入氢离子,就相当于存在了硝酸,将亚硫酸根离子氧化为硫酸根离子,与钡离子形成不可溶的硫酸钡沉淀,也可能含有亚硫酸根离子.
解答:解:A.酸性高锰酸钾能将二氧化硫在水溶液中氧化成硫酸,自身还原为无色的二价锰离子,是酸性高锰酸钾的氧化性的体现,同时体现的是二氧化硫的还原性,故A错误;
B.氨气溶于水NH3+H2O?NH3?H2O?NH4++OH-,水溶液呈碱性,则能使湿润的红色石蕊试纸变蓝,故B正确;
C.酸性氧化物与碱反应生成盐和水,瓷坩埚成分中含二氧化硅,能和氢氧化钠发生反应2NaOH+SiO2═Na2SiO3+H2O,故C错误;
D.因为加入的是硝酸钡,溶液中存在了硝酸根离子,再加入盐酸时引入氢离子,就相当于存在了硝酸,可将亚硫酸根离子氧化为硫酸根离子,与钡离子形成不可溶的硫酸钡沉淀,所以原溶液中也可能含有亚硫酸离子,故D错误;
故选B.
B.氨气溶于水NH3+H2O?NH3?H2O?NH4++OH-,水溶液呈碱性,则能使湿润的红色石蕊试纸变蓝,故B正确;
C.酸性氧化物与碱反应生成盐和水,瓷坩埚成分中含二氧化硅,能和氢氧化钠发生反应2NaOH+SiO2═Na2SiO3+H2O,故C错误;
D.因为加入的是硝酸钡,溶液中存在了硝酸根离子,再加入盐酸时引入氢离子,就相当于存在了硝酸,可将亚硫酸根离子氧化为硫酸根离子,与钡离子形成不可溶的硫酸钡沉淀,所以原溶液中也可能含有亚硫酸离子,故D错误;
故选B.
点评:本题以有关实验操作为载体考查了元素化合物的性质,明确酸性高锰酸钾与二氧化硫的反应原理、掌握氨气的性质、了解陶瓷能与氢氧化钠反应以及硫酸根离子的检验是解答本题的关键,D硫酸根离子的干扰检验是易错点,题目难度中等.

练习册系列答案
相关题目
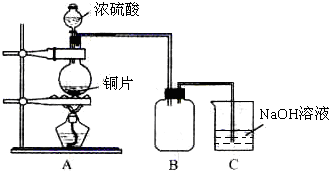
 某课外兴趣小组为探究铜跟浓硫酸的反应情况,设计了右图所示装置进行有关实验:
某课外兴趣小组为探究铜跟浓硫酸的反应情况,设计了右图所示装置进行有关实验: