题目内容
Ⅰ.实验室要用98%(ρ=1.84g?cm-3)的硫酸配制3.68mol?L-1的硫酸溶液480mL
(1)需准确量取98%的硫酸______mL.
(2)准确量取一定体积的98%的硫酸后,要配制3.68mol?L-1的硫酸溶液480mL,必须用到的实验仪器是(填写序号):______.
①500mL量筒 ②烧杯 ③1000mL容量瓶 ④500mL 容量瓶 ⑤天平
⑥胶头滴管 ⑦锥形瓶 ⑧玻璃棒 ⑨酸式滴定管
(3)若配制3.68mol?L-1的硫酸溶液的其他操作均正确,但出现下列错误操作,将使所配制的硫酸溶液浓度偏低的是______.
A.将稀释的硫酸溶液转移至容量瓶后,未洗涤烧杯和玻璃棒.
B.烧杯内的稀硫酸未冷却至室温就转移至容量瓶中
C.用胶头滴管向容量瓶中加水时溶液凹面高于容量瓶刻度,此时立即用滴管将瓶内液体吸出,使溶液凹液面与刻度相切.
D.用胶头滴管加水时,视线高于刻线读数
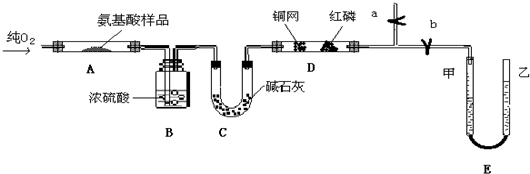
Ⅱ.实验室用燃料法测定某种氨基酸(CxHyOzNp)的分子式组成,取Wg该种氨基酸放在纯氧中充分燃烧,生成CO2、H2O和N2.现用如图所示装置置进行实验(铁架台、铁夹、酒精灯等未画出).请回答有关问题: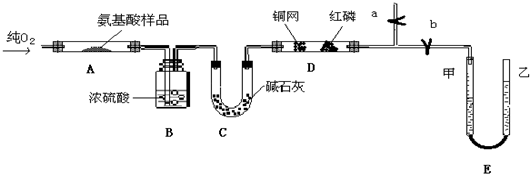
(1)实验开始时,首先打开止水夹a,关闭止水夹b,通入一段时间的氧气,这样做的目的是______,之后关闭止水夹a.
(2)由装置B、C可分别确定待测氨基酸中含有的______和______质量.
(3)E装置的作用是测量______的体积,并由此确定待测氨基酸中含有的______的质量,为了较准确地测量该气体的体积.在读反应前后甲管中液面的读数求其差值的过程中,应注意______(填代号).
a、视线与凹液面最低处相平
b、等待片刻,待乙管中液面不再上升时,立刻读数
c、读数时应上下移动乙管,使甲、乙两管液面相平
d、读数时不一定使甲、乙两管液面相平
(4)实验中测定的哪一数据可能不准确______其理由是______
(5)严格地说,按上述方案只能确定氨基酸的______.若要确定此氨基酸的分子式,还要测定该氨基酸的______.
解:Ⅰ.(1)设需要98%H2SO4的体积为VmL,根据溶液稀释前后溶质质量不变则,VmL×1.84g/cm3×98%=0.5L×3.68mol/L×98g/mol,解得V=100ml,所以溶液的体积为100ml,
故答案为:100;
(2)配制顺序是:计算→量取→稀释、冷却→移液→定容→摇匀→装瓶→贴签,一般用量筒量取(用到胶头滴管)称量,在烧杯中稀释,冷却后转移到500mL容量瓶中,并用玻璃棒引流,转移完毕,用少量蒸馏水洗涤烧杯及玻璃棒2~3次并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,使溶液的凹液面的最低点与刻线相平,塞好瓶塞,反复上下颠倒摇匀.所以仪器有烧杯、玻璃棒、100mL量筒、500mL容量瓶、胶头滴管,故答案为:②④⑥⑧;
(3)A.因烧杯内壁沾有溶质,将稀释的硫酸溶液转移至容量瓶后,未洗涤烧杯和玻璃棒,溶质的质量减小,浓度减少,故A正确;
B.在烧杯中稀释浓硫酸时,未等溶液恢复至室温就转移到容量瓶中,一旦溶液冷却下来,体积偏小,浓度偏大,故B错误;
C.用胶头滴管向容量瓶中加水时凹液面高于容量瓶刻度,此时立即用滴管将瓶内液体吸出,使溶液凹液面与刻度相切,因吸出的液体中含有溶质,溶质的质量减少,浓度减少,故C正确;
D.用胶头滴管加水时,视线高于刻线读数,溶液的液面高于刻度线,溶液的体积偏小,浓度偏大,故D错误;
故选:AC;
Ⅱ.(1)装置的空气中含有N2,影响生成氮气的体积测定,需将装置中的N2排净,故答案为:将装置中的N2排净;
(2)装置B内盛放浓硫酸,吸收生成的水,根据装置B增重,确定Wg该种氨基酸中含氢元素质量,装置C内盛放碱石灰,吸收生成的二氧化碳,根据装置C增重,确定Wg该种氨基酸中含碳元素质量,故答案为:H元素;C元素;
(3)利用排水法测定氮气的体积,确定Wg该种氨基酸中含氮元素质量.读氮气体积时应注意上下移动乙管,使甲、乙两管液面相平,以保证管内压强应与外界大气压相等,视线应与凹液面最低处相平,故答案为:N2;N元素;ac;
(4)为保证氨基酸完全燃烧需通过量的氧气,利用铜网和氧气在加热条件下反应除去未反应完氧气,以防止影响N2的体积的测定,但无法保证完全除去未反应的氧气,
故答案为:N2的体积;多余的O2在D中没有被吸收完全;
(5)该原理只能测出Wg该种氨基酸所含C元素、H元素、O元素的质量,据此可以确定其原子个数比,确定其最简式.若要确定分子式还需测定该氨基酸的相对分子质量.
故答案为:最简式;相对分子质量.
分析:Ⅰ.(1)根据稀释前后溶质的质量不变来计算出溶液的体积;
(2)根据配制一定物质的量浓度溶液的步骤:计算→量取→稀释、冷却→移液→定容→摇匀→装瓶→贴签,确定需要的仪器;
(3)根据c= 分析操作对溶质的物质的量或对溶液的体积的影响判断;
分析操作对溶质的物质的量或对溶液的体积的影响判断;
(4)根据配制时,一旦出现的错误操作,必须重新配制.
Ⅱ.该实验原理为:Wg该种氨基酸放在纯氧中充分燃烧,生成CO2、H2O和N2.通过测定CO2、H2O和N2的质量,确定分子中三种元素原子个数比,由此确定最简式.
(1)利用排水法测定氮气的体积,确定Wg该种氨基酸中含氮元素质量;
(2)装置B内盛放浓硫酸,吸收生成的水,根据装置B增重,确定Wg该种氨基酸中含氢元素质量;
装置C内盛放碱石灰,吸收生成的二氧化碳,根据装置C增重,确定Wg该种氨基酸中含碳元素质量;
(3)E装置的作用是测定氮气的体积;
(4)为保证氨基酸完全燃烧需通过量的氧气;
(5)该原理只能测出Wg该种氨基酸所含C元素、H元素、O元素的质量,据此可以确定其原子个数比.若要确定分子式还需测定该氨基酸的相对分子质量.
点评:本题考查了一定物质的量浓度溶液的配制的计算、步骤以及误差分析,利用燃烧法确定有机物分子组成的知识,难度不大,根据原子守恒法来求解有机物分子组成解答,难度不大,关键在于理解实验原理.
故答案为:100;
(2)配制顺序是:计算→量取→稀释、冷却→移液→定容→摇匀→装瓶→贴签,一般用量筒量取(用到胶头滴管)称量,在烧杯中稀释,冷却后转移到500mL容量瓶中,并用玻璃棒引流,转移完毕,用少量蒸馏水洗涤烧杯及玻璃棒2~3次并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,使溶液的凹液面的最低点与刻线相平,塞好瓶塞,反复上下颠倒摇匀.所以仪器有烧杯、玻璃棒、100mL量筒、500mL容量瓶、胶头滴管,故答案为:②④⑥⑧;
(3)A.因烧杯内壁沾有溶质,将稀释的硫酸溶液转移至容量瓶后,未洗涤烧杯和玻璃棒,溶质的质量减小,浓度减少,故A正确;
B.在烧杯中稀释浓硫酸时,未等溶液恢复至室温就转移到容量瓶中,一旦溶液冷却下来,体积偏小,浓度偏大,故B错误;
C.用胶头滴管向容量瓶中加水时凹液面高于容量瓶刻度,此时立即用滴管将瓶内液体吸出,使溶液凹液面与刻度相切,因吸出的液体中含有溶质,溶质的质量减少,浓度减少,故C正确;
D.用胶头滴管加水时,视线高于刻线读数,溶液的液面高于刻度线,溶液的体积偏小,浓度偏大,故D错误;
故选:AC;
Ⅱ.(1)装置的空气中含有N2,影响生成氮气的体积测定,需将装置中的N2排净,故答案为:将装置中的N2排净;
(2)装置B内盛放浓硫酸,吸收生成的水,根据装置B增重,确定Wg该种氨基酸中含氢元素质量,装置C内盛放碱石灰,吸收生成的二氧化碳,根据装置C增重,确定Wg该种氨基酸中含碳元素质量,故答案为:H元素;C元素;
(3)利用排水法测定氮气的体积,确定Wg该种氨基酸中含氮元素质量.读氮气体积时应注意上下移动乙管,使甲、乙两管液面相平,以保证管内压强应与外界大气压相等,视线应与凹液面最低处相平,故答案为:N2;N元素;ac;
(4)为保证氨基酸完全燃烧需通过量的氧气,利用铜网和氧气在加热条件下反应除去未反应完氧气,以防止影响N2的体积的测定,但无法保证完全除去未反应的氧气,
故答案为:N2的体积;多余的O2在D中没有被吸收完全;
(5)该原理只能测出Wg该种氨基酸所含C元素、H元素、O元素的质量,据此可以确定其原子个数比,确定其最简式.若要确定分子式还需测定该氨基酸的相对分子质量.
故答案为:最简式;相对分子质量.
分析:Ⅰ.(1)根据稀释前后溶质的质量不变来计算出溶液的体积;
(2)根据配制一定物质的量浓度溶液的步骤:计算→量取→稀释、冷却→移液→定容→摇匀→装瓶→贴签,确定需要的仪器;
(3)根据c=
 分析操作对溶质的物质的量或对溶液的体积的影响判断;
分析操作对溶质的物质的量或对溶液的体积的影响判断;(4)根据配制时,一旦出现的错误操作,必须重新配制.
Ⅱ.该实验原理为:Wg该种氨基酸放在纯氧中充分燃烧,生成CO2、H2O和N2.通过测定CO2、H2O和N2的质量,确定分子中三种元素原子个数比,由此确定最简式.
(1)利用排水法测定氮气的体积,确定Wg该种氨基酸中含氮元素质量;
(2)装置B内盛放浓硫酸,吸收生成的水,根据装置B增重,确定Wg该种氨基酸中含氢元素质量;
装置C内盛放碱石灰,吸收生成的二氧化碳,根据装置C增重,确定Wg该种氨基酸中含碳元素质量;
(3)E装置的作用是测定氮气的体积;
(4)为保证氨基酸完全燃烧需通过量的氧气;
(5)该原理只能测出Wg该种氨基酸所含C元素、H元素、O元素的质量,据此可以确定其原子个数比.若要确定分子式还需测定该氨基酸的相对分子质量.
点评:本题考查了一定物质的量浓度溶液的配制的计算、步骤以及误差分析,利用燃烧法确定有机物分子组成的知识,难度不大,根据原子守恒法来求解有机物分子组成解答,难度不大,关键在于理解实验原理.

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案
相关题目
实验室要用98%(密度为1.84g.cm-3)的硫酸配制3.68mol/L的硫酸溶液500ml。
(1)需准确量取98%的硫酸 ml。
(2)要配制3.68mol/L的硫酸溶液500ml,必须用到的仪器是(填写序号) 。
①500ml量筒 ②烧杯 ③1000ml容量瓶 ④500ml容量瓶 ⑤天平 ⑥胶头滴管 ⑦锥形瓶⑧玻璃棒
(3)若配制3.68mol/L的硫酸溶液的其它操作均正确,但出现下列错误操作,将使所配制的硫酸溶液浓度偏低的是 。
| A.将稀释的硫酸溶液转移至容量瓶后,未洗涤烧杯和玻璃棒 |
| B.将烧杯内的稀硫酸向容量瓶内转移时,因操作不当使部分稀硫酸溅出瓶外 |
| C.用胶头滴管向容量瓶中加水时凹液面高于容量瓶刻度,此时立即用滴管将瓶内液体吸出,使溶液凹液面与刻度相切 |
| D.用胶头滴管向容量瓶中加水时,仰视观察溶液凹液面与容量瓶刻度相切 |