题目内容
14.用电子式表示下列物质:(1)Cl2:
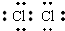 ;
;(2)N2:
 .
.(3)钙离子:Ca2+;
(4)铵根离子:
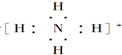 .
.(5)氢氧根离子:
 ;
;(6)过氧根离子:
 .
.
分析 (1)氯气中两个氯原子共用1对电子;
(2)氮气分子中两个氮原子共用3对电子;
(3)钙原子失去2个电子生成钙离子,电子式及其阳离子符号;
(4)铵根离子中4个氢原子与氮原子个共用1对电子;
(5)氢氧根离子带有1个单位负电荷,氢原子与氧原子共用1对电子;
(6)过氧根离子带有2个单位负电荷,两个氧原子之间共用1对电子;
解答 解:(1)Cl2分子两个氯原子共用1对电子,各原子满足8电子稳定结构,电子式为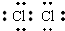 ;
;
故答案为: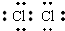 ;
;
(2)氮气分子中两个氮原子共用3对电子,电子式为:氮气的电子式为 ;
;
故答案为: ;
;
(3)钙原子失去2个电子生成钙离子,电子式及其阳离子符号,电子式:Ca2+;
故答案为:Ca2+;
(4)铵根离子中4个氢原子与氮原子个共用1对电子,电子式为: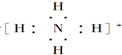 ;
;
故答案为: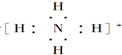 ;
;
(5)氢氧根离子带有1个单位负电荷,氢原子与氧原子共用1对电子,电子式为: ;
;
故答案为: ;
;
(6)过氧根离子为带有2个单位负电荷的离子,离子中存在一个O-O共价键,过氧根离子正确的电子式为: ;
;
故答案为: ;
;
点评 本题考查常见化学用语使用,明确电子式书写原则和方法是解题关键,主要是考查学生对常见化学用语的熟悉掌握程度,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5.下列关系正确的是( )
| A. | 熔点:正戊烷>2,2一二甲基戊烷>2,3一二甲基丁烷>丙烷 | |
| B. | 密度:CCl4>H2O>苯 | |
| C. | 同质量的物质燃烧耗O2量:丙炔>乙烷>乙烯>乙炔>甲烷 | |
| D. | 同物质的量物质燃烧耗O2量:已烷>环已烷>苯>苯甲酸 |
9.下列反应中,不属于取代反应的是( )
| A. | 在催化剂存在条件下苯与溴反应制溴苯 | |
| B. | 苯与浓硝酸、浓硫酸混合共热制取硝基苯 | |
| C. | 在催化剂存在条件下,乙烯与氯化氢反应制氯乙烷 | |
| D. | 葡萄糖与银氨溶液反应 |
19.乙烯可通过石油裂解获得.下列有关乙烯性质的说法错误的是( )
| A. | 在常温常压下为液体 | B. | 能使酸性KMnO4溶液褪色 | ||
| C. | 可自身加成形成聚乙烯 | D. | 能使溴的CCl4溶液褪色 |
3.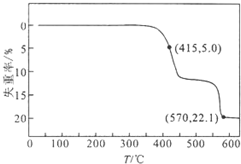 HCOONa加热分解时,固体失重率与温度的关系如图所示,发生的反应有:
HCOONa加热分解时,固体失重率与温度的关系如图所示,发生的反应有:
2HCOONa$\frac{\underline{\;\;△\;\;}}{\;}$Na2C2O4+H2↑①
2HCOONa$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2↑+CO↑②
Na2C2O4$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO↑③
下列说法正确的是( )
 HCOONa加热分解时,固体失重率与温度的关系如图所示,发生的反应有:
HCOONa加热分解时,固体失重率与温度的关系如图所示,发生的反应有:2HCOONa$\frac{\underline{\;\;△\;\;}}{\;}$Na2C2O4+H2↑①
2HCOONa$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2↑+CO↑②
Na2C2O4$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO↑③
下列说法正确的是( )
| A. | T<415℃,只有反应①发生 | |
| B. | 反应①、②不可能同时发生 | |
| C. | 570℃<T<600℃时,残留固体的主要成分是Na2CO3 | |
| D. | 残留固体中的m(Na2C2O4)=m(Na2CO3)时,反应①、③的反应速率相等 |
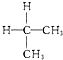 与
与 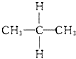
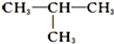
 ;
;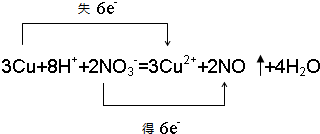 ,在这反应中该强酸展现酸性,氧化性.
,在这反应中该强酸展现酸性,氧化性.