题目内容
A~J是中学化学中常见的化学物质,它们之间的相互转化关系如下列框图所示(部分反应的产物未列出)。
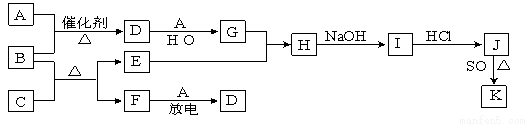
已知:A、F为无色气体单质,B为无色具有刺激性气味的碱性气体,C为黑色氧化物,E为红色金属单质。请回答下列问题:
(1)D的化学式为 ;F的电子式为 。
(2)B和C反应的化学方程式为 。该反应中生成1molF时,转移的电子数为 mol
(3)E与G的稀溶液反应的离子方程式为: 。
(4)J、K是同种金属的不同氯化物,K为白色沉淀。写出SO2还原J生成K的离子方程式 。
练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
10.下列关于氯气的叙述中不正确的是( )
| A. | 氯气溶于水形成纯净物-----氯水 | |
| B. | 实验室制取氯气后可以用向上排空气法收集 | |
| C. | 有氯气参与的反应可以用石灰乳做尾气处理 | |
| D. | 氧化性和毒性都属于氯气的化学性质 |
9.下列说法中正确的是( )
| A. | ⅠA族元素都是金属性很强的金属元素 | |
| B. | F是非金属性最强的元素 | |
| C. | 同族元素中得电子能力越强的电子层数越多 | |
| D. | 元素周期表中最右一列的元素通常具有强氧化性和可变化合价 |
6.设 NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 在5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$2HNO3+4N2↑+9H2O中,生成28 g N2时转移电子的数目为7.5 NA | |
| B. | 16.2 g纤维素完全燃烧,产生CO2分子的数目约为0.6 NA | |
| C. | 电解饱和食盐水产生11.2 L H2,则产生OH-的数目为0.1 NA | |
| D. | 1 L 0.1 mol•L-1NaHCO3溶液中含有HCO3-的数目为0.1 NA |
13.足量的金属锌与一定量稀硫酸反应,既能加快反应速率又不影响氢气的量.下列方法可行的是:( )
①加热 ②加入少量醋酸钠晶体 ③加入食盐水 ④加入少量浓硫酸 ⑤加入少量硫酸铜晶体 ⑥加入少量石墨 ⑦加入少量铜粉 ⑧加入少量镁粉.
①加热 ②加入少量醋酸钠晶体 ③加入食盐水 ④加入少量浓硫酸 ⑤加入少量硫酸铜晶体 ⑥加入少量石墨 ⑦加入少量铜粉 ⑧加入少量镁粉.
| A. | ①④⑤⑥⑦ | B. | ①⑤⑥⑦⑧ | C. | ②③④⑧ | D. | ①④⑤⑥⑦⑧ |
X、Y、Z、W为四种短周期主族元素,它们在周期表中的相对位置如图所示。Z元素原子核外K层与M层电子数相等。下列说法中正确的是 ( )
|
| X | Y |
Z | W |
|
|
A.Y元素最高价氧化物对应的水化物化学式为H2YO3
B.原子半径由小到大的顺序为:Y<X<W<Z
C.室温下,Z和W的单质均能溶于浓硝酸
D.X、Z两种元素的氧化物中所含化学键类型相同



 g C.
g C.  g D.
g D.  g
g bZ(g),反应达到平衡后,测得X的转化
bZ(g),反应达到平衡后,测得X的转化 率为50% 。而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的3/4,则a和b的数值可能是
率为50% 。而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的3/4,则a和b的数值可能是