题目内容
4.化学与环境保护、工业生产、生活等密切相关.下列说法正确的是( )| A. | 用于制作集成电路板的酚醛树脂是天然高分子化合物 | |
| B. | 食盐、食醋、食用油均可用作食品添加剂,都属于有机物 | |
| C. | 碳酸钡、碳酸氢钠、氢氧化铝均可作为抗酸药物使用 | |
| D. | 神舟10号飞船所用太阳能电池板的材料是单晶硅 |
分析 A.酚醛树脂是合成高分子化合物;
B.食盐为无机物;
C.钡离子有毒;
D.硅晶体属于半导体,能制作太阳能电池.
解答 解:A.酚醛树脂是合成高分子化合物,天然高分子化合物有淀粉、纤维素和蛋白质,故A错误;
B.食醋、食用油属于有机物,而食盐为无机物,故B错误;
C.碳酸钡和盐酸反应生成有毒的钡离子,不能用作抗酸药物,故C错误;
D.硅位于金属和非金属分界线处,硅晶体属于半导体,能制作太阳能电池,故D正确.
故选D.
点评 本题综合考查物质的结构与性质,为高频考点,侧重于学生的双基的考查,有利于培养学生良好的科学素养,提高学习的积极性,难度不大.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目
19.已烯雌酚(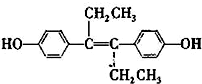 )是一种激素类药物,下列说法不正确的是( )
)是一种激素类药物,下列说法不正确的是( )
 )是一种激素类药物,下列说法不正确的是( )
)是一种激素类药物,下列说法不正确的是( )| A. | 已烯雌酚的分子式为C18H20O2,它为芳香族化合物 | |
| B. | 已烯雌酚分子中一定有16个碳原子共平面 | |
| C. | 1 mol已烯雌酚可以与5 mol Br2发生反应 | |
| D. | 已烯雌酚能发生加成、取代、氧化、加聚、酯化反应 |
20.某微粒用${\;}_{Z}^{A}$Rn+表示,下列关于这种微粒的叙述正确的是( )
| A. | 所含质子数Z+A | B. | 所含电子数Z+n | C. | 所含中子数 A-Z | D. | 质量数Z |
9.下列物质既能与盐酸反应又能与氢氧化钠溶液反应( )
①Al ②Al2O3③NaHCO3④Al(OH)3⑤SiO2.
①Al ②Al2O3③NaHCO3④Al(OH)3⑤SiO2.
| A. | ①③⑤ | B. | ②④⑤ | C. | ①②④⑤ | D. | ①②③④ |
16.中药狼把草的成分之一M具有消炎杀菌作用,M的结构如图所示,则叙述正确的是( )
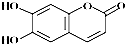

| A. | M的分子式为C9H8O4 | |
| B. | 1 mol M最多能与2 molBr2发生反应 | |
| C. | M与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H4O5Na4 | |
| D. | 1 mol M与足量NaHCO3反应能生成2 mol CO2 |
13.高中化学教材中有很多重要的演示或改编实验,就下列提供的几套装置回答有关问题:

(一)对于实验装置Ⅰ:
(1)用装置Ⅰ完成Al与NaOH溶液反应的实验,并验证生成的气体产物,在b中点燃气体之前,应该先进行验纯,验纯的具体操作为用小试管收集一试管氢气,点燃,听声音,若发出轻微的“噗”的声音,则说明氢气已纯,或发出尖锐的爆鸣声则说明氢气不纯.
(2)用装置Ⅰ还可以完成Na与乙醇反应及气体产物的检验实验:
Na与乙醇反应,理论上有H2生成,若将燃烧后的小烧杯倒转过来,迅速加入澄清石灰水,振荡,发现石灰水变浑浊,原因是氢气中混有乙醇蒸气.
(二)装置Ⅱ用于探究Cl2的漂白性和氧化性:
(3)仪器a的名称为分液漏斗
(4)关闭K1、打开K2,D中的现象为无明显变化.
(5)E中发生反应的离子方程式为SO32-+Cl2+H2O=SO42-+2Cl-+2H+;检验E中有无SO42-生成,用到的试剂有盐酸、氯化钡(填化学式).
(6)整个装置Ⅱ的明显不足之处在于没有尾气吸收装置.
(三)运用装置Ⅲ探究反应速率的影响因素:
(7)该组实验的目的是比较不同浓度的草酸对反应速率的影响;表中V=9mL
(8)有同学观察实验①过程中产生气泡的快慢,得出以下变化(如图甲):

则图甲中AB段变化的主要原因是锰离子对反应有催化作用;另有别的实验小组在完成Zn粒与稀硫酸反应的实验过程中,观察产生氢气的体积与时间的关系,有类似于图甲的规律,如图乙所示,则CD段变化的主要原因是使温度升高,反应速率增大.

(一)对于实验装置Ⅰ:
(1)用装置Ⅰ完成Al与NaOH溶液反应的实验,并验证生成的气体产物,在b中点燃气体之前,应该先进行验纯,验纯的具体操作为用小试管收集一试管氢气,点燃,听声音,若发出轻微的“噗”的声音,则说明氢气已纯,或发出尖锐的爆鸣声则说明氢气不纯.
(2)用装置Ⅰ还可以完成Na与乙醇反应及气体产物的检验实验:
Na与乙醇反应,理论上有H2生成,若将燃烧后的小烧杯倒转过来,迅速加入澄清石灰水,振荡,发现石灰水变浑浊,原因是氢气中混有乙醇蒸气.
(二)装置Ⅱ用于探究Cl2的漂白性和氧化性:
(3)仪器a的名称为分液漏斗
(4)关闭K1、打开K2,D中的现象为无明显变化.
(5)E中发生反应的离子方程式为SO32-+Cl2+H2O=SO42-+2Cl-+2H+;检验E中有无SO42-生成,用到的试剂有盐酸、氯化钡(填化学式).
(6)整个装置Ⅱ的明显不足之处在于没有尾气吸收装置.
(三)运用装置Ⅲ探究反应速率的影响因素:
| 试管编号 | 0.01mol/LKMnO4 | 0.5mol/LH2SO4 | 0.2mol/LH2C2O4 | H2O | 褪色时间/s |
| ① | 4mL | 5mL | 2mL | VmL | t1 |
| ② | 4mL | 5mL | 4mL | 7mL | t2 |
| ③ | 4mL | 5mL | 6mL | 5mL | t3 |
(8)有同学观察实验①过程中产生气泡的快慢,得出以下变化(如图甲):

则图甲中AB段变化的主要原因是锰离子对反应有催化作用;另有别的实验小组在完成Zn粒与稀硫酸反应的实验过程中,观察产生氢气的体积与时间的关系,有类似于图甲的规律,如图乙所示,则CD段变化的主要原因是使温度升高,反应速率增大.
14.下列反应中,属于氧化还原反应又属于置换反应的是( )
| A. | 3NO2+H2O=2HNO3+NO | B. | Cl2+H2O=HCl+HClO | ||
| C. | Na2O+H2O=2NaOH | D. | Fe+CuSO4=Cu+FeSO4 |
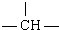

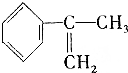 、液溴、浓硫酸和其他无机试剂,请用5个化学方程式表示下列转化过程:
、液溴、浓硫酸和其他无机试剂,请用5个化学方程式表示下列转化过程: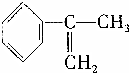 →
→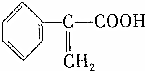
 ;
;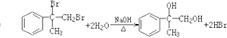 ;
; ;
; ;
;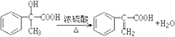 .
.