题目内容
现有标准状况下氨气521L,将其溶于1L水制得密度为0.9g/cm3的氨水,计算该氨水的物质的量浓度为 (计算结果保留小数点后一位).
考点:物质的量浓度的相关计算
专题:物质的量浓度和溶解度专题
分析:NH3溶于水后虽然大部分生成NH3?H2O,但在计算时,仍以NH3作为氨水中的溶质,根据n=
计算氨气的物质的量,根据m=nM计算氨气质量,根据m=ρV计算水的质量,溶液质量=氨气质量+水的质量,根据V=
计算溶液体积,再根据c=
计算氨水的物质的量浓度.
| V |
| Vm |
| m |
| ρ |
| n |
| V |
解答:
解:标况下,521L氨气的物质的量=
=
mol,
氨气的质量=
mol×17g/mol=
g,
水的质量=1L×1000g/L=1000g,
溶液的体积=
=
L,
所得氨水的物质的量浓度=
=15.0mol/L,
故答案为:15.0mol/L.
| 521L |
| 22.4L/mol |
| 521 |
| 22.4 |
氨气的质量=
| 521 |
| 22.4 |
| 521×17 |
| 22.4 |
水的质量=1L×1000g/L=1000g,
溶液的体积=
1000g+
| ||
| 900g/L |
| 22400+521×17 |
| 22.4×900 |
所得氨水的物质的量浓度=
| ||
|
故答案为:15.0mol/L.
点评:本题考查物质的量浓度计算,难度不大,侧重对物质的量浓度定义考查,计算溶液的体积是关键.

练习册系列答案
相关题目
下列溶液,pH>7的是( )
| A、KNO3 |
| B、CH3COONa |
| C、NaHSO4 |
| D、AlCl3 |
下列物质中不可能由一种元素组成的是( )
| A、单质 | B、氧化物 |
| C、化合物 | D、混合物 |
将二氧化碳通入Ba(OH)2稀溶液中,能正确表示其导电能力变化的是( )
A、 |
B、 |
C、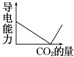 |
D、 |
某种酯的结构可表示为:CmH2m+1COOCnH2n+1,其中m+n=5,该酯的一种水解产物经催化氧化可转化成它的另一种水解产物,则原来的酯是( )
| A、丙酸乙酯 | B、乙酸乙酯 |
| C、丁酸甲酯 | D、丙酸丙酯 |
