题目内容
7. Cl2和H2O2是高中阶段最常见的两种氧化剂,经查阅资料Cl2氧化能力强于H2O2,能将H2O2氧化.为了验证某小组学生设计了如下图所示的实验装置进行实验(夹持装置略去).
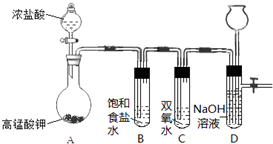
Cl2和H2O2是高中阶段最常见的两种氧化剂,经查阅资料Cl2氧化能力强于H2O2,能将H2O2氧化.为了验证某小组学生设计了如下图所示的实验装置进行实验(夹持装置略去).已知:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O
试管B中饱和食盐水的主要作用是除去Cl2中混有的HCl
请回答下列问题.
(1)试管C发生反应的化学方程式是Cl2+H2O2=2HCl+O2.
(2)试管D中NaOH溶液的作用是吸收多余的氯气.
(3)将浓盐酸注入圆底烧瓶A,当装置中的空气基本排尽后关闭D中止水夹,反应一段时间后试管D中的现象为试管D中液面下降,长颈漏斗中液面上升,试管D中的气体检验方法为该气体能使带火星的木条复燃,证明是氧气.
(4)有的同学对上述实验中D试管中的气体来源产生质疑,你认为可能的来源有2H2O2=2H2O+O2↑或Cl2+H2O?HCl+HClO、2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑(用方程式回答).对于质疑可以采用对比实验来解决.
分析 (1)氯气与双氧水反应生成氯化氢和氧气;
(2)氯气有毒,直接排放会引起空气污染,氯气能够与氢氧化钠溶液反应,被吸收;
(3)氯气和过氧化氢反应生成氧气,氧气难溶于水,根据氧气具有助燃性进行验证氧气;
(4)过氧化化氢分解生成氧气,氯气和水反应生成盐酸和次氯酸,次氯酸分解生成氧气.
解答 解:(1)氯气与双氧水反应生成氯化氢和氧气,化学方程式为:Cl2+H2O2=2HCl+O2,
故答案为:Cl2+H2O2=2HCl+O2;
(2)氯气有毒,直接排放会引起空气污染,氯气能够与氢氧化钠溶液反应,被氢氧化钠溶液吸收,所以可以用氢氧化钠吸收过量的氯气;
故答案为:吸收多余的氯气;
(3)Cl2+H2O2=2HCl+O2,当关闭止水夹,反应一段时间后试管D中因氧气不断增多,气体压强增大,所以试管D中液面下降,长颈漏斗中液面上升,氧气使带火星的木条复燃,可用此法验证氧气,
故答案为:试管D中液面下降,长颈漏斗中液面上升;该气体能使带火星的木条复燃,证明是氧气;
(4)试管D中气体来源可能为过氧化氢的分解:2H2O2=2H2O+O2↑,也可能为氯气氯气和水反应生成盐酸和次氯酸,次氯酸分解生成氧气:Cl2+H2O?HCl+HClO、2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑,
故答案为:2H2O2=2H2O+O2↑或Cl2+H2O?HCl+HClO、2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑.
点评 本题通过氯气与双氧水氧化性强弱比较实验,考查了氯气的实验室制备、净化、性质检验等,熟悉物质的性质是解题关键,题目难度中等,试题考查了学生的实验探究能力和分析能力.

练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
17.下列关于物质用途的叙述中不正确的是( )
| A. | Na2O2可用作呼吸面具中的供氧剂 | |
| B. | 硅胶多孔,吸水能力强,可做食品干燥剂 | |
| C. | Al(OH)3可作治疗胃酸过多的一种药剂 | |
| D. | 四氧化三铁俗称铁红,可用于作油漆、红色涂料 |
18.下列关于物质性质的说法不正确的是( )
| A. | HCl气体能使湿润的蓝色石蕊试纸变红 | |
| B. | 通常状况下,NO2是无色的气体 | |
| C. | 铝单质可与氢氧化钠溶液反应生成氢气 | |
| D. | 铁单质与浓硝酸加热时能发生反应 |
2.下列说法错误的是( )
| A. | 用酸性KMnO4溶液鉴别CH3CH3和CH2=CH2 | |
| B. | 将盛有等体积CH4和Cl2的大试管倒扣在水槽中光照,试管内不能充满液体 | |
| C. | 用NaOH溶液除去乙酸乙酯中的少量乙酸 | |
| D. | 用NaOH溶液和新制Cu(OH)2悬浊液检验淀粉在稀H2SO4作用下是否水解 |
12.下列物质互为同分异构体的是( )
| A. | 12C与13C | B. | O2与O3 | C. | 苯与甲苯 | D. | 1-丙醇与2-丙醇 |
16.下列单质或化合物性质的描述正确的是( )
| A. | 常温常压下,一氧化氮能与空气中的氧气直接化合 | |
| B. | SiO2与酸、碱均不反应 | |
| C. | Na2O、Na2O2组成元素相同,两化合物都为碱性氧化物 | |
| D. | NO2通入FeSO4溶液中始终无明显现象 |
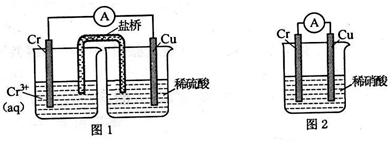 铬化学丰富多彩,由于铬光泽度好,常将铬镀在其他金属表面,同铁、镍组成各 种性能的不锈钢,CrO3大量地用于电镀工业中.
铬化学丰富多彩,由于铬光泽度好,常将铬镀在其他金属表面,同铁、镍组成各 种性能的不锈钢,CrO3大量地用于电镀工业中.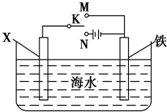 ,可以模拟铁的电化学防护.若 X 为碳棒,为减缓铁的腐蚀,开关 K 应置于N处.若 X 为锌,开关K 置于N或M处.
,可以模拟铁的电化学防护.若 X 为碳棒,为减缓铁的腐蚀,开关 K 应置于N处.若 X 为锌,开关K 置于N或M处.