题目内容
17.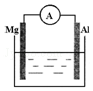 如图所示装置中,金属镁、铝和电流表通过导线相连:
如图所示装置中,金属镁、铝和电流表通过导线相连:(1)若烧杯中溶液为稀硫酸,两极的电极反应式为:
负极Mg-2e-=Mg2+;
正极2H++2e-=H2↑.
(2)若烧杯中溶液为氢氧化钠溶液,两极的电极反应式为:
负极Al+4OH--3e-=AlO2-+2H2O;
正极2H2O+2e-=H2↑+2OH-.
分析 根据自发的氧化还原反应能设计成原电池,失电子的一极是负极,得到电子的是正极,结合电极上反应物分析.
解答 解:(1)镁、铝和稀硫酸构成了原电池,金属镁做负极,电极反应:Mg-2e-=Mg2+,金属铝为正极,溶液中的2H+得到电子发生还原反应,电极反应为:2H++2e-=H2↑;
故答案为:Mg-2e-=Mg2+;2H++2e-=H2↑.
(2)镁、铝和NaOH溶液构成了原电池,铝易失电子作负极,电极反应式为Al+4OH--3e-=AlO2-+2H2O,正极上水得电子发生还原反应,电极反应式为2H2O+2e-=H2↑+2OH-,
故答案为:Al+4OH--3e-=AlO2-+2H2O;2H2O+2e-=H2↑+2OH-.
点评 本题考查了原电池原理,正确判断原电池正负极是解本题关键,根据各个电极上发生的反应以及电解质溶液分析解答,题目难度不大.

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目
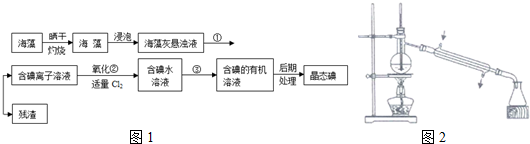
7.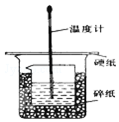 某实验小组设计用50mL 1.0mol/L盐酸跟50mL 1.1mol/L 氢氧化钠溶液在如图装置中进行中和反应.在大烧杯底部垫碎泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平.然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过.通过测定反应过程中所放出的热量可计算中和热.试回答下列问题:
某实验小组设计用50mL 1.0mol/L盐酸跟50mL 1.1mol/L 氢氧化钠溶液在如图装置中进行中和反应.在大烧杯底部垫碎泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平.然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过.通过测定反应过程中所放出的热量可计算中和热.试回答下列问题:
(1)本实验中还缺少一个仪器,其名称是环形玻璃搅拌棒.在大小烧杯中填充泡沫塑料的作用是温隔热,防止热量散失.
(2)该实验小组做了三次实验,每次取溶液各50mL,并记录下原始数据(见表).
已知盐酸、NaOH溶液密度近似为1.00g/cm3,中和后混合液的比热容为:c=4.18×10-3kJ/(g•℃),则写出该反应的热化学方程式(离子方程式)H+(aq)+OH-(aq)=H2O(l)△H=-56.0kJ/mol (△H值保留到小数点后1位).
(3)若用等浓度的醋酸与NaOH溶液反应,则测得的中和热会比(2)测出的△H偏大(填“偏大”、“偏小”或“不变”).
(4)在中和热测定实验中存在用水洗涤温度计上的盐酸后再用温度计测定NaOH溶液温度的步骤,若无此
操作步骤,则测得的中和热△H会偏大(填“偏大”、“偏小”或“不变”).
 某实验小组设计用50mL 1.0mol/L盐酸跟50mL 1.1mol/L 氢氧化钠溶液在如图装置中进行中和反应.在大烧杯底部垫碎泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平.然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过.通过测定反应过程中所放出的热量可计算中和热.试回答下列问题:
某实验小组设计用50mL 1.0mol/L盐酸跟50mL 1.1mol/L 氢氧化钠溶液在如图装置中进行中和反应.在大烧杯底部垫碎泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平.然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过.通过测定反应过程中所放出的热量可计算中和热.试回答下列问题:(1)本实验中还缺少一个仪器,其名称是环形玻璃搅拌棒.在大小烧杯中填充泡沫塑料的作用是温隔热,防止热量散失.
(2)该实验小组做了三次实验,每次取溶液各50mL,并记录下原始数据(见表).
| 实验序号 | 起始温州 t1/℃ | 终止温度(t2)/℃[ | 温差 (t2-t1)/℃ | ||
| 盐酸 | NaOH溶液 | 平均值 | |||
| 1 | 25.1 | 24.9 | 25.0 | 31.6 | 6.6 |
| 2 | 25.1 | 25.1 | 25.1 | 31.8 | 6.7 |
| 3 | 25.1 | 25.1 | 25.1 | 31.9 | 6.8 |
(3)若用等浓度的醋酸与NaOH溶液反应,则测得的中和热会比(2)测出的△H偏大(填“偏大”、“偏小”或“不变”).
(4)在中和热测定实验中存在用水洗涤温度计上的盐酸后再用温度计测定NaOH溶液温度的步骤,若无此
操作步骤,则测得的中和热△H会偏大(填“偏大”、“偏小”或“不变”).
8.下列无法证明某酸HA是弱酸的实验方案是( )
| A. | 室温下,测得某HA溶液中c(HA)=0.01mol•L-1 | |
| B. | 碳酸钠溶液中滴入0.1mol•L-1的HA溶液,产生大量无色气体 | |
| C. | 室温下测得某HA溶液的pH=a,用蒸馏水稀释100倍测得溶液pH=b,且b-a<2 | |
| D. | 室温下,测得0.1mol•L-1HA溶液的pH>1,证明HA是弱酸 |
5.(1)下列每组分别给出了两个量.其中可以组成一个物质的量公式的组有 (填编号)①④⑤
(2)在标准状况下:①6.72LCH4,②3.01×1023个HCl分子,③13.6gH2S,④0.2molNH3
下列对这四种气体的描述正确的是(填写代号)ABCD
A.质量②>③>①>④B.密度②>③>④>①C体积②>③>①>④D.氢原子数①>③>④>②
| ① | ② | ③ | ④ | ⑤ |
| 物质所含的微粒数 | 固体体积 | 溶液的质量百分比浓度 | 标准状况下气体的摩尔体积 | 非标准状况下某物质的质量 |
| 阿伏加德罗常数 | 固体密度 | 溶液体积 | 标准状况下气体的体积 | 物质的摩尔质量 |
下列对这四种气体的描述正确的是(填写代号)ABCD
A.质量②>③>①>④B.密度②>③>④>①C体积②>③>①>④D.氢原子数①>③>④>②
12.下列化学用语表示正确的是( )
| A. | 氯化钠的电子式为Na:$\underset{\stackrel{•}{C}}{•}\underset{\stackrel{•}{l}}{•}$: | |
| B. | 次氯酸的电子式H:$\underset{\stackrel{•}{C}}{•}\underset{\stackrel{•}{l}}{•}$: | |
| C. | 二氧化碳的结构式为O=C=O | |
| D. | NaHCO3的电离方程式为NaHCO3=Na++H++CO32- |
 2NH3(g)△H=-92kJ/mol.
2NH3(g)△H=-92kJ/mol.