题目内容
设NA是阿伏伽德罗常数的数值,下列说法正确的是( )
| A、1mol Na+离子含有的核外电子数为NA |
| B、1mol Cl2与足量的铁反应,转移的电子数为3NA |
| C、标准状况下,22.4L的CCl4中含有的CCl4分子数为NA |
| D、常温下,10L pH=13的NaOH溶液中含有的OH-离子数为NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、钠原子失去一个电子析出,核外有10个电子;
B、1mol Cl2与足量的铁反应生成氯化铁,电子转移依据全部反应的氯气计算;
C、标准状况四氯化碳不是气体;
D、依据PH计算溶液中氢氧根离子浓度,结合n=CV=
计算;
B、1mol Cl2与足量的铁反应生成氯化铁,电子转移依据全部反应的氯气计算;
C、标准状况四氯化碳不是气体;
D、依据PH计算溶液中氢氧根离子浓度,结合n=CV=
| N |
| NA |
解答:
解:A、钠原子失去一个电子析出,核外有10个电子,1mol Na+离子含有的核外电子数为10NA,故A错误;
B、1mol Cl2与足量的铁反应生成氯化铁,电子转移依据全部反应的氯气计算电子转移2mol×NA=2NA,故B错误;
C、标准状况四氯化碳不是气体,22.4L的CCl4中物质的量不是1mol,故C错误;
D、依据PH计算溶液中氢氧根离子浓度,结合n=CV=
计算,10L pH=13的NaOH溶液中含有的OH-离子数=
mol/L×10L×NA=NA,故D正确;
故选D.
B、1mol Cl2与足量的铁反应生成氯化铁,电子转移依据全部反应的氯气计算电子转移2mol×NA=2NA,故B错误;
C、标准状况四氯化碳不是气体,22.4L的CCl4中物质的量不是1mol,故C错误;
D、依据PH计算溶液中氢氧根离子浓度,结合n=CV=
| N |
| NA |
| 10-14 |
| 10-13 |
故选D.
点评:本题考查了阿伏伽德罗常数的分析应用,主要是 摩尔体积的条件应用,氧化还原反应电子转移计算,掌握基础是关键,题目较简单.

练习册系列答案
 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案
相关题目
某氨水中c(NH4+)=0.5mol/L时达到电离平衡,若向其中加入c(NH4+)=0.5mol/L的NH4Cl溶液后,NH3?H2O的电离程度将( )
| A、减少 | B、不变 |
| C、增大 | D、无法判断 |
2003年诺贝尔物理学奖颁给三位对超导和超流理论方面进行研究并作出先驱性贡献的科学家.低温液态的42He和32He具有超流体特性.关于42He说法错误的是( )
| A、质子数为2 |
| B、电子数为2 |
| C、质量数为4 |
| D、中子数为4 |
下列物质不能发生酯化反应的是( )
| A、酒精 |
| B、冰醋酸 |
| C、乙醛 |
| D、甲醇(CH3OH) |
下列化学方程式或离子方程式正确的是( )
A、苯酚钠溶液中通入少量二氧化碳的离子方程式: |
B、制备酚醛树脂的化学方程式: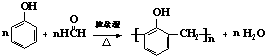 |
C、丙烯聚合成聚丙烯的化学方程式: |
| D、丙烯与溴化氢主反应为:CH3-CH=CH2+HBr→CH3-CH2-CHBr |
下列关于有机物的说法中,正确的一组是
①溴乙烷、乙酸乙酯在一定的条件下都能发生水解反应
②“乙醇汽油”是在汽油里加入适量乙醇而成的一种燃料,它是一种新型化合物
③乙烯和SO2都能使溴水褪色,但褪色的原理不同
④石油的分馏、裂化和煤的干馏都是化学变化
⑤淀粉遇碘酒变蓝色;在加热条件下葡萄糖能与新制氢氧化铜悬浊液反应
⑥汽油、柴油和果糖都是碳氢化合物,完全燃烧只生成CO2和H2O( )
①溴乙烷、乙酸乙酯在一定的条件下都能发生水解反应
②“乙醇汽油”是在汽油里加入适量乙醇而成的一种燃料,它是一种新型化合物
③乙烯和SO2都能使溴水褪色,但褪色的原理不同
④石油的分馏、裂化和煤的干馏都是化学变化
⑤淀粉遇碘酒变蓝色;在加热条件下葡萄糖能与新制氢氧化铜悬浊液反应
⑥汽油、柴油和果糖都是碳氢化合物,完全燃烧只生成CO2和H2O( )
| A、①③⑤ | B、②④⑥ |
| C、①②⑤ | D、③④⑥ |
设NA为阿伏加德罗常数,下列说法不正确的是( )
| A、标准状况下22.4L Cl2和H2混合气体原子数为2NA |
| B、1mol Na2O2和足量的水完全反应,转移的电子数为NA |
| C、1mol金刚石中含共价键数目为4NA |
| D、电解食盐水若产生2g氢气,则转移的电子数目为2NA |