题目内容
已知反应
①Cl2+2KBr=2KCl+Br2
②KClO3 +6HCl=3Cl2+KCl +3H2O
③2KBrO3 +Cl2=Br2 + 2KClO3
下列说法正确的是
- A.上述三个反应都有单质生成,所以都是置换反应
- B.氧化性由强到弱顺序为 KBrO3>KClO3>Cl2>Br2
- C.反应②中还原剂与氧化剂的物质的量之比为6:1
- D.③中1mol还原剂反应则氧化剂得到电子的物质的量为2mol
B
一种单质和一种化合物反应,生成另外一种单质和化合物的反应是置换反应,所以②不是置换反应,A不正确。根据氧化还原反应中还原剂的氧化性大于氧化产物的可判断,B是正确的。反应②中,根据电子的得失守恒可知还原剂与氧化剂的物质的量之比为5︰1,C不正确。③中1mol还原剂失去电子的物质的量是2×5=10mol,则氧化剂就应该得到10mol电子,D不正确。答案选B。
一种单质和一种化合物反应,生成另外一种单质和化合物的反应是置换反应,所以②不是置换反应,A不正确。根据氧化还原反应中还原剂的氧化性大于氧化产物的可判断,B是正确的。反应②中,根据电子的得失守恒可知还原剂与氧化剂的物质的量之比为5︰1,C不正确。③中1mol还原剂失去电子的物质的量是2×5=10mol,则氧化剂就应该得到10mol电子,D不正确。答案选B。

练习册系列答案
相关题目
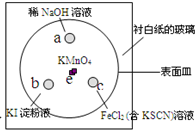 (2011?崇明县一模)如图,化学实验的微型化可有效减少污染,实现化学实验的绿色要求.某学生在一块衬白纸的玻璃片的不同位置分别加一滴含酚酞的NaOH溶液(a)、浓度为0.1mol/L KI淀粉溶液(b)、FeCl2(含KSCN)溶液(c),并在e处放置少量KMnO4晶体,向KMnO4晶体上滴加几滴浓盐酸后立即用表面皿盖好,形成一个气室.
(2011?崇明县一模)如图,化学实验的微型化可有效减少污染,实现化学实验的绿色要求.某学生在一块衬白纸的玻璃片的不同位置分别加一滴含酚酞的NaOH溶液(a)、浓度为0.1mol/L KI淀粉溶液(b)、FeCl2(含KSCN)溶液(c),并在e处放置少量KMnO4晶体,向KMnO4晶体上滴加几滴浓盐酸后立即用表面皿盖好,形成一个气室. 根据如图反应框图填空,已知反应①是工业上生产化合物D的反应,反应⑤是实验室鉴定化合物E的反应.
根据如图反应框图填空,已知反应①是工业上生产化合物D的反应,反应⑤是实验室鉴定化合物E的反应. 红磷 P(s)和 Cl2(g)发生反应生成 PCl3(g)和 PCl5(g).反应过程和能量关系如图所示(图中的△H表示生成 1 mol 产物的数据).
红磷 P(s)和 Cl2(g)发生反应生成 PCl3(g)和 PCl5(g).反应过程和能量关系如图所示(图中的△H表示生成 1 mol 产物的数据). HCl+HClO,写出该反应化学平衡常数的表达式
HCl+HClO,写出该反应化学平衡常数的表达式 
 HCl+HClO,写出该反应化学平衡常数的表达式
HCl+HClO,写出该反应化学平衡常数的表达式