题目内容
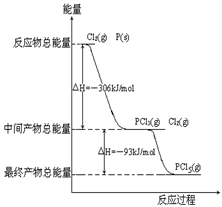
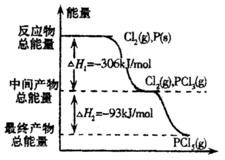
 红磷 P(s)和 Cl2(g)发生反应生成 PCl3(g)和 PCl5(g).反应过程和能量关系如图所示(图中的△H表示生成 1 mol 产物的数据).
红磷 P(s)和 Cl2(g)发生反应生成 PCl3(g)和 PCl5(g).反应过程和能量关系如图所示(图中的△H表示生成 1 mol 产物的数据).根据上图回答下列问题:
(1)P和Cl2反应生成PCl3的热化学方程式是
P(s)+
Cl2(g)═PCl3(g)△H=-306kJ?mol-1
| 3 |
| 2 |
P(s)+
Cl2(g)═PCl3(g)△H=-306kJ?mol-1
.| 3 |
| 2 |
(2)PCl5分解成 PCl3和Cl2的热化学方程式是
PCl5(g)═PCl3(g)+Cl2(g)△H=+93kJ?mol-1
PCl5(g)═PCl3(g)+Cl2(g)△H=+93kJ?mol-1
.(3)P和Cl2分两步反应生成1molPCl5的△H3=
-399kJ?mol-1
-399kJ?mol-1
,P和Cl2一步反应生成1molPCl5的△H4等于
等于
△H3(填“大于”、“小于”或“等于”).(4)PCl5 与足量水充分反应,最终生成两种酸,已知反应前后各元素化合价不变,其化学方程式是
PCl5+4H2O═H3PO4+5HCl
PCl5+4H2O═H3PO4+5HCl
.分析:(1)根据图象得出反应物、生成物以及反应热=生成物的总能量-反应物的总能量,然后依据书写热化学方程式的原则书写;
(2)根据图象得出反应物、生成物以及反应热=生成物的总能量-反应物的总能量,然后依据书写热化学方程式的原则书写;
(3)根据盖斯定律分析,根据反应物的总能量、中间产物的总能量以及最终产物的总能量,结合化学方程式以及热化学方程式的书写方法解答,注意盖斯定律的应用;
(4)PCl5与足量水充分反应,最终生成磷酸和盐酸.
(2)根据图象得出反应物、生成物以及反应热=生成物的总能量-反应物的总能量,然后依据书写热化学方程式的原则书写;
(3)根据盖斯定律分析,根据反应物的总能量、中间产物的总能量以及最终产物的总能量,结合化学方程式以及热化学方程式的书写方法解答,注意盖斯定律的应用;
(4)PCl5与足量水充分反应,最终生成磷酸和盐酸.
解答:解:(1)根据图示可知:P(s)+
Cl2(g)═PCl3(g),反应物的总能量大于生成物的总能量,该反应是放热反应,反应热为△H=-306 kJ/mol,则热化学方程式为:P(s)+
Cl2(g)═PCl3(g)△H=-306 kJ/mol,
故答案为:P(s)+
Cl2(g)═PCl3(g)△H=-306kJ?mol-1;
(2)根据图示可知:Cl2(g)+PCl3(g)═PCl5(g),中间产物的总能量大于最终产物的总能量,该反应是放热反应,△H=生成物总能量-反应物总能量=-93 kJ/mol;所以PCl5(g)═PCl3(g)+Cl2(g)是吸热反应;热化学方程式为PCl5(g)═PCl3(g)+Cl2(g)△H=+93 kJ/mol,
故答案为:PCl5(g)═PCl3(g)+Cl2(g)△H=+93kJ?mol-1;
(3)根据盖斯定律,P和Cl2分两步反应和一步反应生成PCl5的△H应该是相等的,P和Cl2分两步反应生成1 molPCl5的热化学方程式:
P(s)+32Cl2(g)═PCl3(g)△H1=-306 kJ/mol,
Cl2(g)+PCl3(g)═PCl5(g)△H2=-93 kJ/mol;
P和Cl2一步反应生成1molPCl5的△H3=-306 kJ/mol+(-93 kJ/mol)=-399 kJ/mol,
由图象可知,P和Cl2分两步反应生成1molPCl5的△H3=-306kJ/mol-(+93kJ/mol)=399kJ/mol,根据盖斯定律可知,反应无论一步完成还是分多步完成,生成相同的产物,反应热相等,则P和Cl2一步反应生成1molPCl5的反应热等于P和Cl2分两步反应生成1molPCl5的反应热,
故答案为:-399kJ?mol-1;等于;
(5)PCl5与足量水充分反应,最终生成两种酸:磷酸和盐酸,由原子守恒可知化学方程式为PCl5+4H2O═H3PO4+5HCl,
故答案为:PCl5+4H2O═H3PO4+5HCl.
| 3 |
| 2 |
| 3 |
| 2 |
故答案为:P(s)+
| 3 |
| 2 |
(2)根据图示可知:Cl2(g)+PCl3(g)═PCl5(g),中间产物的总能量大于最终产物的总能量,该反应是放热反应,△H=生成物总能量-反应物总能量=-93 kJ/mol;所以PCl5(g)═PCl3(g)+Cl2(g)是吸热反应;热化学方程式为PCl5(g)═PCl3(g)+Cl2(g)△H=+93 kJ/mol,
故答案为:PCl5(g)═PCl3(g)+Cl2(g)△H=+93kJ?mol-1;
(3)根据盖斯定律,P和Cl2分两步反应和一步反应生成PCl5的△H应该是相等的,P和Cl2分两步反应生成1 molPCl5的热化学方程式:
P(s)+32Cl2(g)═PCl3(g)△H1=-306 kJ/mol,
Cl2(g)+PCl3(g)═PCl5(g)△H2=-93 kJ/mol;
P和Cl2一步反应生成1molPCl5的△H3=-306 kJ/mol+(-93 kJ/mol)=-399 kJ/mol,
由图象可知,P和Cl2分两步反应生成1molPCl5的△H3=-306kJ/mol-(+93kJ/mol)=399kJ/mol,根据盖斯定律可知,反应无论一步完成还是分多步完成,生成相同的产物,反应热相等,则P和Cl2一步反应生成1molPCl5的反应热等于P和Cl2分两步反应生成1molPCl5的反应热,
故答案为:-399kJ?mol-1;等于;
(5)PCl5与足量水充分反应,最终生成两种酸:磷酸和盐酸,由原子守恒可知化学方程式为PCl5+4H2O═H3PO4+5HCl,
故答案为:PCl5+4H2O═H3PO4+5HCl.
点评:本题考查热化学方程式的书写、反应热的计算、盖斯定律计算等知识,解题中需注意:热化学方程式中没有标注各物质的聚集状态,各物质的物质的量与反应热没有呈现对应的比例关系.

练习册系列答案
相关题目
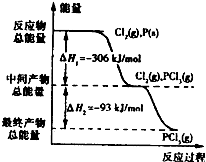 如图是红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)的反应过程和能量关系图.其中PCl5(g)分解成PCl3(g)和Cl2(g)的反应是一个可逆反应,温度T℃时,在密闭容器中加入0.6mol PCl5,达平衡时,PCl5还剩0.45mol,其分解率为α,则下列推断不正确的是( )
如图是红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)的反应过程和能量关系图.其中PCl5(g)分解成PCl3(g)和Cl2(g)的反应是一个可逆反应,温度T℃时,在密闭容器中加入0.6mol PCl5,达平衡时,PCl5还剩0.45mol,其分解率为α,则下列推断不正确的是( )| A、α等于25% | B、若升高温度,平衡时PCl5的分解率小于α | C、若初始时加入0.6mol PCl3和0.6 mol Cl2,以相同条件进行反应,则平衡时PCl3转化率为3α | D、PCl5分解的热化学方程式为:PCl5(g)?PCl3(g)+Cl2(g)△H=-93kJ?mol-1 |