题目内容
标准状况下,1.68L无色可燃性气体在足量氧气中完全燃烧,将产生的CO2和H2O蒸气及剩余的O2全部通过如图所示的装置,得到如下表所列的实验数据(假设生成的气体全部被吸收).

根据实验数据填空:
(1)该气体完全燃烧生成水的质量为 g,生成CO2的质量为 g.
(2)若原气体是单一气体,通过计算推断它的分子式.
(3)若原气体是两种等物质的量的气体的混合物,其中只有一种是烃,请写出它们的分子式(只要求写出一组).
| 实验前 | 实验后 | |
| 甲的质量/g | 101.1 | 103.8 |
| 乙的质量/g | 82.0 | 88.6 |

根据实验数据填空:
(1)该气体完全燃烧生成水的质量为
(2)若原气体是单一气体,通过计算推断它的分子式.
(3)若原气体是两种等物质的量的气体的混合物,其中只有一种是烃,请写出它们的分子式(只要求写出一组).
考点:有关有机物分子式确定的计算,有关混合物反应的计算
专题:计算题
分析:(1)浓硫酸增重的为水的质量、乙中碱石灰增重的为二氧化碳的质量;
(2)若为单一气体,该气体为烃,根据有机物的物质的量、C、H的物质的量计算出其分子式;
(3)根据(2)的计算结果及题干信息判断可能的混合物组成.
(2)若为单一气体,该气体为烃,根据有机物的物质的量、C、H的物质的量计算出其分子式;
(3)根据(2)的计算结果及题干信息判断可能的混合物组成.
解答:
解:(1)根据题意,甲中浓硫酸增加的质量为水的质量:103.8g-101.1g=2.7g,
碱石灰可吸收二氧化碳,增加的质量:88.6g-82.0g=6.6g,
故答案为:2.7;6.6;
(2)标准状况下1.68L气体的物质的量为:
=0.075mol,
有机物燃烧生成水的物质的量为:
=0.15mol,
有机物燃烧生成二氧化碳的质量为:
=0.15mol,
该有机物中含有C、H原子数为:n(C)=
=2、n(H)=
=4,
若为单一气体,则该气体为乙烯,分子式为:C2H4,
答:若原气体是单一气体,其分子式为C2H4;
(3)若原气体是两种等物质的量的气体的混合物,其中分子中含有C、H为:C2H4,其中只有一种是烃,
当另一种为氢气时,平均分子式为C2H4,则该烃为C4H6,该气体组成为:C4H6和H2;
当另一种气体为CO时,平均分子式为C2H4,则该烃为C3H8,该气体组成为:C3H8和CO,
答:若原气体是两种等物质的量的气体的混合物,其中只有一种是烃,它们的分子式为C4H6和H2(或C3H8和CO或C3H6和CH2O).
碱石灰可吸收二氧化碳,增加的质量:88.6g-82.0g=6.6g,
故答案为:2.7;6.6;
(2)标准状况下1.68L气体的物质的量为:
| 1.68L |
| 22.4L/mol |
有机物燃烧生成水的物质的量为:
| 2.7g |
| 18g/mol |
有机物燃烧生成二氧化碳的质量为:
| 6.6g |
| 44g/mol |
该有机物中含有C、H原子数为:n(C)=
| 0.15mol |
| 0.075mol |
| 0.15mol×2 |
| 0.075mol |
若为单一气体,则该气体为乙烯,分子式为:C2H4,
答:若原气体是单一气体,其分子式为C2H4;
(3)若原气体是两种等物质的量的气体的混合物,其中分子中含有C、H为:C2H4,其中只有一种是烃,
当另一种为氢气时,平均分子式为C2H4,则该烃为C4H6,该气体组成为:C4H6和H2;
当另一种气体为CO时,平均分子式为C2H4,则该烃为C3H8,该气体组成为:C3H8和CO,
答:若原气体是两种等物质的量的气体的混合物,其中只有一种是烃,它们的分子式为C4H6和H2(或C3H8和CO或C3H6和CH2O).
点评:本题考查了确定有机物分子式的计算,题目难度中等,注意掌握确定有机物分子式的方法,明确质量守恒定律在化学计算中的应用,试题侧重考查学生的分析、理解能力及化学计算能力.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
某实验小组只领取下列仪器或用品:铁架台、铁圈、三角架、石棉网、烧杯、分液漏斗、酒精灯、玻璃棒、量筒、蒸发皿、圆底烧瓶、火柴.只应用上述仪器或用品,不能进行的实验操作是( )
| A、蒸发 | B、萃取 | C、过滤 | D、蒸馏 |
下列分离和提纯的实验,所选用的方法和仪器不正确的是( )
| 序号 | A | B | C | D |
| 实验目的 | 食盐水与泥沙分离 | 制取蒸馏水 | 分离水和植物油 | 从浓食盐水中 得到氯化钠晶体 |
| 分离方法 | 萃取 | 蒸馏 | 分液 | 蒸发 |
| 选用仪器 | 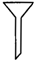 | 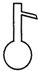 |  |  |
| A、A | B、B | C、C | D、D |
衡量一个国家化学工业发展水平标志的是下列哪一种物质的产量( )
| A、钢铁 |
| B、石油和煤 |
| C、乙烯 |
| D、CO2的排放量 |