题目内容
13.pH=12的NaAlO2溶液,水电离的c(OH-)=0.01mol/.分析 NaAlO2是强碱弱酸盐,促进水电离,溶液中氢氧根离子就是水电离出的氢氧根离子.
解答 解:NaAlO2是强碱弱酸盐,促进水电离,溶液中氢氧根离子就是水电离出的氢氧根离子,因此水电离出的c(OH-)=$\frac{10{\;}^{-14}}{10{\;}^{-12}}$mol/L=0.01mol/L,
故答案为:0.01mol/L.
点评 本题考查了pH的简单计算,明确含有弱根离子的盐对水电离的影响是解本题关键,难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案
相关题目
4.下列各组性质比较中,正确的是( )
①酸性:HClO4>HBrO4>HIO4
②碱性:Ba(OH)2>Mg(OH)2>B(OH)2
③氧化性:F>Si>O
④还原性:HCl<H2S<SiH4.
①酸性:HClO4>HBrO4>HIO4
②碱性:Ba(OH)2>Mg(OH)2>B(OH)2
③氧化性:F>Si>O
④还原性:HCl<H2S<SiH4.
| A. | ①②③ | B. | ②③④ | C. | ①②④ | D. | ①③④ |
1.DDT是人类合成得到的第一种有机农药,它的结构简式如图所示,有关它的说法正确的是( )
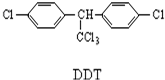

| A. | 它属于芳香烃 | B. | 分子式为C14H8Cl5 | ||
| C. | 1mol该物质能与6mol H2加成 | D. | 分子中最多可能有28个原子共面 |
8.下列各项与化学平衡移动原理无关的是( )
| A. | 收集氯气用排饱和食盐水的方法 | |
| B. | 加催化剂,使N2和H2在一定的条件下转化为NH3 | |
| C. | 可用浓氨水和氢氧化钠固体快速制取氨气 | |
| D. | 加压条件下有利于SO2和O2反应生成SO3 |
5.甲醇是一种重要的化工原料,广泛应用于化工生产,也可直接用作燃料.已知:CH3OH(l)+O2(g)═CO(g)+2H2O(g)△H1=-443.64kJ•mol-1;2CO(g)+O2(g)═2CO2(g)△H2=-566kJ•mol-1.下列说法或热化学方程式正确的是( )
| A. | CO的燃烧热为566kJ•mol-1 | |
| B. | 2 mol CO和1 mol O2的总能量比2 mol CO2的总能量低 | |
| C. | 2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(g)△H=-1453.28kJ•mol-1 | |
| D. | 完全燃烧16g甲醇,生成一氧化碳和水时放出的热量为221.82 kJ |
2.现有部分短周期元素的性质或原子结构如下表:
下列说法正确的是( )
| 元素编号 | 元素性质或原子结构 |
| T | 最外层电子数是次外层电子数的2倍 |
| X | L层有三个未成对电子 |
| Y | L层p电子数比s电子数多两个 |
| Z | 元素的最高正价为+7价 |
| A. | Z离子的结构示意图为: | B. | 分子TY2的键角为180° | ||
| C. | T元素在周期表中的表示为: | D. | XZ3为非极性分子 |
 某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.
某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.