题目内容
8.将碱溶液A、盐溶液B按如下程度进行实验,根据下述现象判断: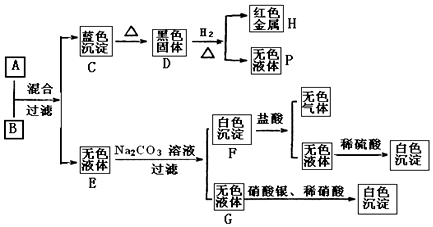
(1)A的化学式Ba(OH)2 B的化学式CuCl2.
(2)完成下列转化的化学方程式,并用单线桥标明电子转移的方向和数目:D→H+P:
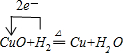
(3)写出下列反应的离子方程式:
A+B:Cu2++2OH-=Cu(OH)2↓
F+盐酸:BaCO3+2H+=Ba2++CO2↑+H2O.
分析 由转化关系图,H为红色金属,H为Cu,C为蓝色沉淀,为Cu(OH)2,加热氢氧化铜时,氢氧化铜分解生成黑色的氧化铜,故D为CuO,氧化铜被氢气还原生成铜和水,所以P为H2O;
碱溶液A+盐溶液B→Cu(OH)2+无色溶液E,B为铜盐,由无色溶液E和碳酸钠溶液反应生成白色沉淀,故G为氯化钠,无色溶液E含有Cl-,故盐溶液B为CuCl2;
F和盐酸反应生成无色气体和无色溶液,白色沉淀F为碳酸盐,该无色溶液和稀硫酸反应生成白色沉淀,故无色溶液含有Ba2+,故白色沉淀为BaCO3,无色溶液E含有Cl-,故E为BaCl2,再结合碱溶液A+盐溶液B→Cu(OH)2+无色溶液E,故A为Ba(OH)2,据此分析解答.
解答 解:由转化关系图,H为红色金属,H为Cu,C为蓝色沉淀,为Cu(OH)2,加热氢氧化铜时,氢氧化铜分解生成黑色的氧化铜,故D为CuO,氧化铜被氢气还原生成铜和水,所以P为H2O;
碱溶液A+盐溶液B→Cu(OH)2+无色溶液E,B为铜盐,由无色溶液E和碳酸钠溶液反应生成白色沉淀,故G为氯化钠,无色溶液E含有Cl-,故盐溶液B为CuCl2;
F和盐酸反应生成无色气体和无色溶液,白色沉淀F为碳酸盐,该无色溶液和稀硫酸反应生成白色沉淀,故无色溶液含有Ba2+,故白色沉淀为BaCO3,无色溶液E含有Cl-,故E为BaCl2,再结合碱溶液A+盐溶液B→Cu(OH)2+无色溶液E,故A为Ba(OH)2,
(1)通过以上分析知,A、B化学式分别为Ba(OH)2、CuCl2,故答案为:Ba(OH)2;CuCl2;
(2)D→H+P为CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O,反应中电子转移数目为2,用“单线桥法”标明电子转移的方向和数目为: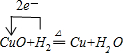 ;
;
故答案为: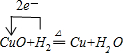 ;
;
(3)A+B反应是氢氧化钡与氯化铜反应生成氢氧化铜与氯化钡,反应离子方程式为:Cu2++2OH-=Cu(OH)2↓;
F+盐酸是碳酸钡与元素反应生成氯化钡、二氧化碳与水,反应离子方程式为:BaCO3+2H+=Ba2++CO2↑+H2O;
故答案为:Cu2++2OH-=Cu(OH)2↓;BaCO3+2H+=Ba2++CO2↑+H2O.
点评 本题考查了无机物的推断,利用物质的某些特殊性质来分析解答,以H为突破口采用正逆相结合的方法进行推断,注意基础知识的总结归纳,题目难度不大.

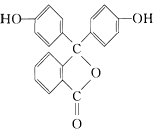
| A. | 1mol酚酞最多与2molNaOH发生中和反应 | |
| B. | 酚酞分子中所有碳原子不可能共平面 | |
| C. | 酚酞结构中有三个苯环,属于芳香烃 | |
| D. | 酚酞的分子式为C20H14O4 |
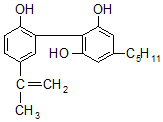
| A. | 该物质属于芳香烃 | |
| B. | 1mol该物质最多能与7molH2加成 | |
| C. | 该物质分子结构中存在7个碳碳双键 | |
| D. | 该物质能使酸性KMnO4溶液褪色 |

| A. | 乙、丙都能发生银镜反应 | |
| B. | 用FeCl3溶液鉴别甲、丙两种有机化合物 | |
| C. | 甲分子中所有碳原子可能共平面 | |
| D. | 甲、乙、丙三种有机化合物均可与NaOH溶液发生反应 |
| A. | ③①②④ | B. | ④③②① | C. | ①④②③ | D. | ②①④③ |

 源生产部分材料。
源生产部分材料。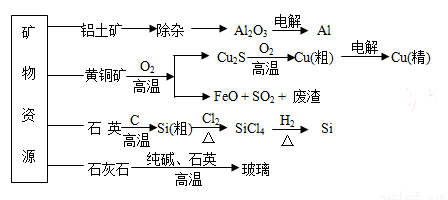
 ,FeO可用作冶炼铁的原料
,FeO可用作冶炼铁的原料 非金属单质一定是氧化剂
非金属单质一定是氧化剂