题目内容
15.常用于分离和提纯的物理方法有:A萃取分液法 B结晶法 C分液法 D蒸馏法 E过滤法
(1)选择实验方法分离下列物质,将分离方法(填字母)填在横线上
①E分离饱和食盐水与沙子的混合物.
②C分离水和汽油的混合物.
③D分离四氯化碳(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物.
④AD从碘的水溶液里提取碘.
(2)分离②和④时均使用的一种仪器在另外实验方法中无需使用,这种仪器是分液漏斗.
(3)上述实验方法中,需使用酒精灯的有BD(填数字编号).
分析 (1)①沙子不溶于水;
②水和汽油分层;
③二者互溶,但沸点不同;
④碘不易溶于水,易溶于有机溶剂;
(2)均使用的一种仪器为分液漏斗;
(3)蒸馏、蒸发需要酒精灯.
解答 解:(1)①沙子不溶于水,则选择过滤法分离,故答案为:E;
②水和汽油分层,则选择分液法分离,故答案为:C;
③二者互溶,但沸点不同,则选择蒸馏法分离,故答案为:D;
④碘不易溶于水,易溶于有机溶剂,则选择萃取、分液,然后蒸馏分离出碘,故答案为:AD;
(2)分离②和④时均使用的一种仪器在另三种实验方法中无需使用,这种仪器是为分液漏斗,故答案为:分液漏斗;
(3)上述实验方法中,需使用酒精灯的有BD,故答案为:BD.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异、混合物分离方法为解答的关键,侧重分析与应用能力的考查,注意实验仪器的使用,题目难度不大.

练习册系列答案
相关题目
9.下列各选项中所述的两个量,前者一定大于后者的是 (各项所处温度都是相同的)( )
| A. | 稀盐酸与稀醋酸的导电性 | |
| B. | 物质的量浓度相等的 (NH4)2Fe(SO4)2溶液和 (NH4)2SO4溶液中NH4+的浓度 | |
| C. | 用量筒量取液体时,仰视的读数和俯视的读数 | |
| D. | 物质的量浓度相等的NaHCO3溶液和Na2CO3溶液中水的电离程度 |
10.核磁共振造影增强剂用于疾病诊断,还可作为药物载体用于疾病的治疗.为磁性纳米晶体材料在生物医学领域的应用提供了更广泛的前景.制备纳米四氧化三铁过程如下:

下列有关叙述不合理的是( )

下列有关叙述不合理的是( )
| A. | 纳米四氧化三铁具有磁性作为药物载体用于疾病的治疗 | |
| B. | 反应③的化学方程式是:6FeOOH+CO=2Fe3O4+3H2O+CO2 | |
| C. | 纳米四氧化三铁分散在适当溶剂中,它与溶液分散质直径相当 | |
| D. | 在反应②环丙胺的作用可能是促进氯化铁水解 |
3.随着核电荷数的递增,氧化性逐渐减弱的一组是( )
| A. | I2、Br2、Cl2、F2 | B. | Li、Na、K、Rb | C. | F2、Cl2、Br2、I2 | D. | F-、Cl-、Br-、I- |
10.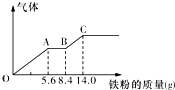 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解9.6g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体).下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解9.6g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体).下列分析或结果错误的是( )
 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解9.6g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体).下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解9.6g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体).下列分析或结果错误的是( )| A. | H2SO4浓度为2.5 mol•L-1 | |
| B. | OA段产生的是NO,AB段的反应为Fe+2Fe3+═3Fe2+,BC段产生氢气 | |
| C. | 第二份溶液中最终溶质为FeSO4 | |
| D. | 原混合酸中NO3-物质的量为0.1 mol |
20.四种主族元素的离子aXm+、bYn+、cZn-和 dRm-具有相同的电子层结构,若m>n,则下列叙述的判断正确的是( )
①a-c=n-m
②元素的原子序数a>b>c>d
③元素非金属性Z>R
④最高价氧化物对应水化物碱性X>Y.
①a-c=n-m
②元素的原子序数a>b>c>d
③元素非金属性Z>R
④最高价氧化物对应水化物碱性X>Y.
| A. | ①②③④ | B. | ①②③ | C. | ②③ | D. | 只有③ |
7.下列说法正确的是( )
| A. | 在高温下,有1 mol Fe与足量的水蒸气反应,转移电子的数目为3NA | |
| B. | 1 mol的羟基与1 mol的氢氧根离子所含电子数均为10NA | |
| C. | 酸性溶液中可能大量存在Na+、ClO?、SO42?、I? | |
| D. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1012的溶液中:NH4+、Al3+、NO3-、Cl-离子组能够大量共存 |
4.下列各组金属只用CuSO4溶液就能确定金属活动性强弱顺序的是( )
| A. | Fe和Zn | B. | Fe和Ag | C. | Ag和Hg | D. | Mg和Zn |
5.下列粒子中,既具有氧化性,又具有还原性的是( )
| A. | Mg | B. | Cu2+ | C. | Fe2+ | D. | Cl- |