题目内容
7.下列说法正确的是( )| A. | 在高温下,有1 mol Fe与足量的水蒸气反应,转移电子的数目为3NA | |
| B. | 1 mol的羟基与1 mol的氢氧根离子所含电子数均为10NA | |
| C. | 酸性溶液中可能大量存在Na+、ClO?、SO42?、I? | |
| D. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1012的溶液中:NH4+、Al3+、NO3-、Cl-离子组能够大量共存 |
分析 A.铁与水蒸气反应生成的是四氧化三铁,产物中铁元素的平均化合价为+$\frac{8}{3}$价;
B.羟基中含有9个电子,氢氧根离子含有10个电子;
C.次氯酸根离子能够氧化碘离子,能够与氢离子结合生成次氯酸;
D.该溶液呈酸性,溶液中存在大量氢离子,四种离子之间不反应,都不与氢离子反应.
解答 解:A.Fe与水蒸气在高温下反应生成四氧化三铁,反应中转移电子的物质的量为:1mol×($\frac{8}{3}$-0)=$\frac{8}{3}$mol,转移电子的数目为$\frac{8}{3}$NA,故A错误;
B.1mol羟基中含有9mol电子,1mol氢氧根离子含有10mol电子,二者含有的电子数不同,故B错误;
C.ClO-、I-之间发生氧化还原反应,ClO-与酸性溶液中的氢离子反应生成次氯酸,在溶液中不能大量共存,故C错误;
D.该溶液中存在大量氢离子,NH4+、Al3+、NO3-、Cl-离子之间不发生反应,都不与氢离子反应,在溶液中能够大量共存,故D正确;
故选D.
点评 本题考查离子共存、物质的量计算,为高考的高频题,题目难度不大,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案
相关题目
2.下列叙述正确的是( )
| A. | 利用高纯硅可以制成光电池,将光能直接转化为电能 | |
| B. | CO、CO2均易于血红蛋白结合而中毒 | |
| C. | SiO2可用于制造光导纤维和半导体 | |
| D. | SiO2和H2O反应可直接制备H2SiO3 |
2.氯化钾溶液中混有少量的硫酸铜,若加入一种试剂能除去硫酸铜,该试剂为( )
| A. | NaOH | B. | AgNO3 | C. | BaCl2 | D. | Ba(OH)2 |
16.下列物质的描述不正确的是( )
| A. | 醇是分子中含有跟链烃基或苯环上的碳结合的羟基的化合物 | |
| B. | 分子中含有碳碳双键的一类链烃叫做烯烃 | |
| C. | 石油的馏分是指石油分馏出来的各种成分,它是混合物 | |
| D. | 煤干馏生成焦炭、煤焦油、焦炉气和粗氨水,属于化学变化 |
17.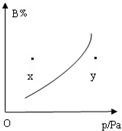 现有mA(s)+nB(g)?pC(g)(正反应放热)的可逆反应,在一定温度下平衡时B的转化率和压强间的关系如图所示,则有关该反应的下列描述中正确的是( )
现有mA(s)+nB(g)?pC(g)(正反应放热)的可逆反应,在一定温度下平衡时B的转化率和压强间的关系如图所示,则有关该反应的下列描述中正确的是( )
 现有mA(s)+nB(g)?pC(g)(正反应放热)的可逆反应,在一定温度下平衡时B的转化率和压强间的关系如图所示,则有关该反应的下列描述中正确的是( )
现有mA(s)+nB(g)?pC(g)(正反应放热)的可逆反应,在一定温度下平衡时B的转化率和压强间的关系如图所示,则有关该反应的下列描述中正确的是( )| A. | m+n<p | B. | n<p | ||
| C. | x点的混合物中v正<v逆 | D. | x点比y点的混合物正反应速度大 |
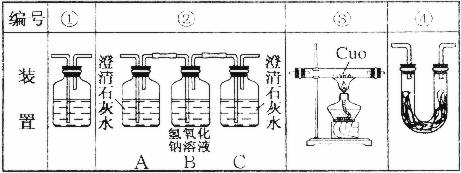
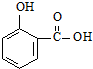 )的沸点与对羟基苯甲酸(
)的沸点与对羟基苯甲酸(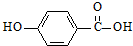 )的沸点相同是由于它们互为同分异构体不正确;邻羟基苯甲醛分子内的羟基与醛基之间即存在氢键(分子内氢键),而对羟基苯甲醛分子之间存在氢键(分子间氢键),与互为同分异构体无关.
)的沸点相同是由于它们互为同分异构体不正确;邻羟基苯甲醛分子内的羟基与醛基之间即存在氢键(分子内氢键),而对羟基苯甲醛分子之间存在氢键(分子间氢键),与互为同分异构体无关.