题目内容
在密闭容器中进行反应X2(气)+3Y2(气) 2Z(气),其中X2,Y2,Z的起始浓度分别是0.1mol/L,0.3mol/L,0.2mol/L.当反应达到平衡时,各物质的浓度可能的是
2Z(气),其中X2,Y2,Z的起始浓度分别是0.1mol/L,0.3mol/L,0.2mol/L.当反应达到平衡时,各物质的浓度可能的是
[ ]
A.c(X2)=0.2mol/L
B.c(Z)=0.5mol/L
C.c(Y2)=0.1mol/L
D.c(X2)=c(Y2)=c(Z)
答案:C
解析:
解析:
|
导解:假设可逆反应正向进行并进行到底,平衡时c(X2)=0,c(Y2)=0,c(Z)=0.4mol/L;假设可逆反应逆向进行并进行到底,平衡时c(X2)=0.2mol/L,c(Y2)=0.6mol/L,c(Z)=0.这就是平衡时各物质的浓度可能的范围:0<c(X2)<0.2,0<c(Y2)<0.6,0<c(Z)<0.4.因为X2和Y2的投料比为1∶3,化学计量数之比也为1∶3,所以c(X2)∶c(Y2)=1∶3. |

练习册系列答案
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案
相关题目
在密闭容器中进行反应:X2(g)+Y2(g)?2Z(g)已知X2、Y2、Z的起始浓度分别为0.1mol?L-1、0.3mol?L-1、0.2mol?L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )
| A、Z为0.35mol?L-1 | B、Y2为0.45mol?L-1 | C、X2为0.2 mol?L-1 | D、Z为0.4mol?L-1 |
(双选).在密闭容器中进行反应X2(g)+Y2(g)?2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol.L-1、0.3mol.L-1、0.2mol.L-1,在一定条件下当反应达到平衡时,各物质的浓度有可能是( )
| A、Z为0.3mol.L-1, | B、X2为0.2mol.L-1, | C、Y2为0.3mol.L-1, | D、Z为0.4mol.L-1, |
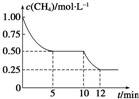 在密闭容器中进行反应CH4(g)+H2O(g)?CO(g)+3H2(g)△H>0,测得c(CH4)随反应时间(t)的变化如图所示.下列判断不正确的是( )
在密闭容器中进行反应CH4(g)+H2O(g)?CO(g)+3H2(g)△H>0,测得c(CH4)随反应时间(t)的变化如图所示.下列判断不正确的是( )| A、10min时,改变的外界条件可能是升高温度 | B、0~10min内,v(H2)=0.15mol?L-1?min-1 | C、恒温下,缩小容器体积,一段时间内v逆>v正 | D、12min时,反应达平衡的本质原因是气体总质量不再变化 |
 (2012?石家庄一模)常温下,A为无色无味液体,B为淡黄色粉末,D、E、G、W为气体,且G的相对分子质量比D大16,各物质间的转化关系如图所示:
(2012?石家庄一模)常温下,A为无色无味液体,B为淡黄色粉末,D、E、G、W为气体,且G的相对分子质量比D大16,各物质间的转化关系如图所示: