题目内容
(16分)软锰矿的主要成分为MnO2,还含有Fe2O3、MgO、Al2O3、CaO等杂质,工业上用软锰矿制取MnSO4·H2O的流程如下:

已知:Fe3+、Al3+、Mn2+和Mg2+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、5.2、10.4、12.4;温度高于27℃时,MnSO4的溶解度随温度的升高而逐渐降低。
(1)“浸出”过程中MnO2转化为Mn2+的离子方程式为________。
(2)“浸出”过程中Fe2O3转化为Fe3+和Fe2+,相关反应的离子方程式为________。
(3)“滤渣1”的主要成分是__________,“调pH至5~6”所加的试剂是_________(填“石灰水”或“稀硫酸”)。
(4)根据下表数据,选择“第2步除杂”所加的物质A(由一种阳离子和一种阴离子组成),物质A的化学式为________。
Ksp 阳离子 | CO32- | F- | OH- |
Ca2+ | 5.0×10-9 | 1.5×10-10 | 4.7×10-6 |
Mg2+ | 3.8×10-6 | 7.4×10-11 | 5.6×10-12 |
Mn2+ | 2.2×10-11 | 5.3×10-3 | 2.1×10-13 |
Zn2+ | 1.2×10-10 | 3.0×10-2 | 6.9×10-17 |
(5)采用“趁热过滤”操作的原因是________。
(1)MnO2+SO2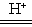 Mn2++SO42-
Mn2++SO42-
(2)Fe2O3+6H+=2Fe3++3H2O;2Fe3++SO2+2H2O=2Fe2++4H++SO42-
(3)Fe(OH)3、Al(OH)3;石灰水 (4)MnF2
(5)防止温度下降时MnSO4H2O溶解,导致产率降低
【解析】
试题分析:(1)浸出过程中MnO2被SO2还原转化为Mn2+的离子方程式为MnO2+SO2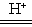 Mn2++SO42-。
Mn2++SO42-。
(2)浸出过程中Fe2O3与酸反应生成铁离子,铁离子被SO2还原转化为亚铁离子,则转化为Fe3+和Fe2+的离子方程式为Fe2O3+6H+=2Fe3++3H2O;2Fe3++SO2+2H2O=2Fe2++4H++SO42-。
(3)双氧水把亚铁离子氧化为铁离子,根据金属阳离子沉淀时的pH值可知pH在5到6之间时生成的沉淀是氢氧化铁和氢氧化铝,及滤渣1的主要成分是Fe(OH)3、Al(OH)3;要增大溶液的pH则需要加入氢氧化钙,硫酸是强酸,不能选择,则调pH至5~6所加的试剂是石灰水。
(4)由于不能引入杂质,则阳离子选择锰离子。又因为要沉淀溶液中的镁离子和钙离子,则A的溶度积常数不能太小,所以根据下表数据可知“第2步除杂”所加的物质A MnF2。
(5)由于温度高于27℃时,MnSO4的溶解度随温度的升高而逐渐降低,所以为防止温度下降时MnSO4·H2O溶解,导致产率降低,因此需要“趁热过滤”。
考点:考查物质制备工艺流程图的分析与应用

 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案X、Y、Z、W四种短周期元素在元素周期表中的相对位置如图所示,这四种元素原子的最外层电子数之和为20,下列判断正确的是
W | X | Y |
Z |
A.四种元素的原子半径:rZ>rX>rY>rW
B.四种元素形成的单质最多有6种
C.四种元素均可与氢元素形成电子总数为18的分子
D.四种元素中,Z的最高价氧化物对应的水化物酸性最强
 阴离子
阴离子

 b时的沉淀成分为BaSO4与Mg (OH) 2
b时的沉淀成分为BaSO4与Mg (OH) 2 




 的一种同分异构体满足下列条件:
的一种同分异构体满足下列条件: