题目内容
12.下列路易斯酸中,酸性最强的是( )| A. | AlCl3 | B. | BF3 | C. | BCl3 | D. | BBr3 |
分析 路易斯从他的电子理论出发,为酸碱作出了更为广泛的定义:可接受一个电子对的物质是酸,可给出一个电子对的物质是碱,越容易接受电子对的,其路易斯酸性越强,据此解答.
解答 解:AlCl3,BX3结构中都存在4原子6电子的大π键,因为硼是第二周期元素,半径较小,易于发生π电子重叠,这是第二周期元素特有的,而Al是第三周期元素,一方面不易形成π键,另一方面,还有空的d轨道,易于接受电子,所以相对路易斯酸性更强,
故选A.
点评 本题考查了物质结构与性质关系,明确元素原子结构及成键方式是解题关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.已知一个某原子的质量是M g,则该原子的摩尔质量是( )
| A. | M•NA | B. | Mg/mol | C. | $\frac{M}{{N}_{A}}$g/mol | D. | M•NA g/mol |
20.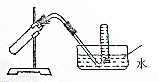 如图装置可用于( )
如图装置可用于( )
 如图装置可用于( )
如图装置可用于( )| A. | 加热NaHCO3制CO2 | B. | 用Cu和稀HNO3反应制NO | ||
| C. | 用NH4Cl与浓NaOH溶液反应制NH3 | D. | 用NaCl于浓H2SO4反应制HCl |
7.下列有关漂白粉的说法正确的是( )
| A. | 漂白粉的有效成分是CaCl2 | |
| B. | 漂白粉和明矾处理自来水的原理是相同的 | |
| C. | 漂白粉最好在弱酸性环境下使用 | |
| D. | 漂白粉因易在空气中氧化而密封保存 |
4.现有以下8种物质:a.铝、b.NaHSO4固体、c.氯化氢、d.SO2、e.Ba(OH)2固体,f.K2co3固体、g.稀硫酸、h.熔融NaNO3
(1)按物质的分类方法填写表格的空白处(填编号)
(2)e与g在水溶液中反应的离子方程式为Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O.
(1)按物质的分类方法填写表格的空白处(填编号)
| 分类标准 | 能导电的物质 | 电解质 | 能电离出H+的物质 |
| 属于该类的物质 | a、g、h | b、c、e、f、h | b、c、g |
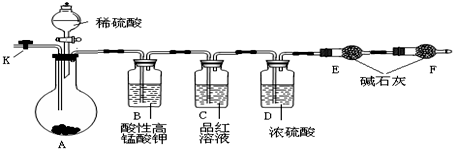
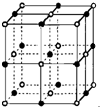 第二周期中碳、氮、氧是构成生命物质的三种主要元素,在生产生活中也有着重要的应用.
第二周期中碳、氮、氧是构成生命物质的三种主要元素,在生产生活中也有着重要的应用.