题目内容
17.在一定条件下,要除去CuCl2溶液中的Fe3+,不能加入下列哪种物质③?①CuO ②Cu(OH)2 ③NaOH ④Cu2(OH)2CO3.
分析 Fe3+易水解生成氢氧化铁沉淀,所加入物质起到调节溶液pH的作用,但不能引入新的杂质.
解答 解:加氢氧化钠虽可起到调节溶液pH的作用,但引入新的杂质,不符合除杂的原则,
Fe3+易水解生成氢氧化铁沉淀,可加入碳酸铜、氧化铜或氢氧化铜、Cu2(OH)2CO3等物质,调节溶液的pH且不引入新的杂质,
故答案为:③.
点评 本题考查盐类水解的原理及应用,为高频考点,侧重于除杂与分离,题目较为基础,解答本题的关键是能把握除杂的原则.

练习册系列答案
相关题目
7.下列变化中不可能通过一步完成的是( )
| A. | Al(OH)3→Al2O3 | B. | Al2O3→Al(OH)3 | C. | Na2O2→NaOH | D. | Na2CO3→NaHCO3 |
5.为除去氯化铜中混有的氯化亚铁得到纯净的氯化铜溶液,常先加入H2O2溶液将Fe2+全部氧化成Fe3+,然后再加入( )
| A. | NaOH溶液 | B. | 氨水 | C. | CuO | D. | KSCN溶液 |
12.下列路易斯酸中,酸性最强的是( )
| A. | AlCl3 | B. | BF3 | C. | BCl3 | D. | BBr3 |
2.下列实验操作及现象与结论对应关系不相符的一组是( )
| 实验 | 现象 | 结论 | |
| A | 将硫酸酸化的H2O2滴入Fe(NO2)2溶液 | 溶液变黄色 | H2O2的氧化性比Fe3+强 |
| B | 等体积pH=2的HX和HY两种酸分别与足量的铁反应,排水法收集气体 | HX放出的氢气多 | HX酸性比HY弱 |
| C | 将ZnS加入水中形成白色悬浊液,再向其中加入CuSO4溶液 | 有黑色沉淀产生 | Ksp(ZnS)>Ksp(CuS) |
| D | 光洁的铁钉放在冷的浓硫酸中 | 无明显现象 | 浓硫酸具有强氧化性 |
| A. | A | B. | B | C. | C | D. | D |
1.室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示.下列说法正确的是( )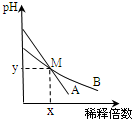

| A. | 取等体积M点的A、B两种碱液加入同浓度的硫酸溶液至恰好完全反应时,所消耗酸溶液的体积相同 | |
| B. | 用醋酸中和A溶液至恰好完全反应时,溶液的pH不一定大于7 | |
| C. | 稀释前两溶液中H+浓度的大小关系:A=10B | |
| D. | 稀释前,A溶液中由水电离出的OH-的浓度大于10-7mol/L |