题目内容
2.氧族元素的各种性质可归纳整理出如表(部分):| 元素 性质 | 8O | 16S | Se | 52Te |
| 单质沸点(℃) | -183 | 444.6 | 685 | 1 390 |
| 主要化合价 | -2 | -2,+4,+6 | -2,+4,+6 | |
| 原子半径(nm) | 0.074 | 0.102 | 0.116 | 0.143 |
| 单质与H2反应 | 点燃易化合 | 加热化合 | 加热难化合 | 不能直接化合 |
(1)S2-的电子式为
 .
.(2)氧元素比硫元素非金属性强(填强或弱).请用化学方程式证明该结论:2H2S+O2=2S↓+2H2O.
分析 (1)S2-的核外有18个电子,最外层有8个电子;
(2)同主族从上到下元素的非金属性逐渐减弱;单质的氧化性越强,其元素的非金属性越强.
解答 解:(1)S2-的核外有18个电子,最外层有8个电子,其电子式为 ,故答案为:
,故答案为: ;
;
(2)同主族从上到下元素的非金属性逐渐减弱,则氧元素比硫元素非金属性强;单质的氧化性越强,其元素的非金属性越强,氧气能把硫化氢氧化为S,其反应方程式为:2H2S+O2=2S↓+2H2O;
故答案为:强;2H2S+O2=2S↓+2H2O.
点评 本题主要考查了氧族元素的性质,考查了类推法的应用,注意把握同主族元素性质的递变规律,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.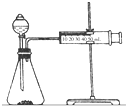 影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究.
影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究.
实验一:甲同学利用Al、Fe、Mg和2mol/L的稀硫酸,设计实验方案研究影响反应速率的因素.
研究的实验报告如下表:
(1)该同学的实验目的是探究反应物本身的性质对反应速率的影响;
要得出正确的实验结论,还需控制的实验条件是温度相同.
(2)乙同学为了更精确地研究浓度对反应速率的影响,利用如图装置同温下进行定量实验,用大小形状相同的Fe分别和0.5mol/L及2mol/L的足量稀H2SO4反应,通过测定和比较同时间内产生氢气的体积可以说明浓度对化学反应速率的影响.
实验二:已知2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+8H2O+10CO2↑,在开始一段时间内,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快.
(1)针对上述现象,某同学认为该反应放热,导致溶液温度上升,反应速率加快.从影响化学反应速率的因素看,你猜想还可能是Mn2+的催化作用的影响.
(2)若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液外,可以在反应一开始时加入B.
A.硫酸钾 B.硫酸锰 C.氯化锰 D.水.
 影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究.
影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究.实验一:甲同学利用Al、Fe、Mg和2mol/L的稀硫酸,设计实验方案研究影响反应速率的因素.
研究的实验报告如下表:
| 实验步骤 | 现象 | 结论 |
| ①分别取等体积的2mol/L的硫酸于试管中;②分别投入大小、形状相同的Al、Fe、Mg | 反应快慢:Mg>Al>Fe | 反应物的性质越活泼,反应速率越快 |
要得出正确的实验结论,还需控制的实验条件是温度相同.
(2)乙同学为了更精确地研究浓度对反应速率的影响,利用如图装置同温下进行定量实验,用大小形状相同的Fe分别和0.5mol/L及2mol/L的足量稀H2SO4反应,通过测定和比较同时间内产生氢气的体积可以说明浓度对化学反应速率的影响.
实验二:已知2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+8H2O+10CO2↑,在开始一段时间内,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快.
(1)针对上述现象,某同学认为该反应放热,导致溶液温度上升,反应速率加快.从影响化学反应速率的因素看,你猜想还可能是Mn2+的催化作用的影响.
(2)若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液外,可以在反应一开始时加入B.
A.硫酸钾 B.硫酸锰 C.氯化锰 D.水.
13.80g密度为ρg.cm-3的CaCl2溶液里含2gCa2+,从中再取出一半的溶液中Cl-的浓度是( )
| A. | $\frac{ρ}{800}$mol•L-1 | B. | 1.25ρmol•L-1 | C. | $\frac{ρ}{1600}$mol•L-1 | D. | 0.63mol•L-1 |
17.检验居室中有甲醛气体,可连续多次抽取居室空气样品,注入到低浓度(1×10-4mol/L)的酸性高锰酸钾溶液中.据此,下列说法正确的是( )
| A. | 最终酸性高锰酸钾溶液褪色 | B. | 反应中甲醛被还原 | ||
| C. | 最终酸性高锰酸钾溶液是红色 | D. | 说明甲醛是具有氧化性的气体 |
7.(1)补充完成表格:(请把序号①-④的答案对应填入横线上)
(2)甲与乙两元素的单质反应生成物的电子式为 .
.
(3)乙元素最高价氧化物对应水化物的化学式为HClO4.
(4)甲单质与水反应的化学方程式为2Na+2H2O=2NaOH+H2↑.
| 元素 | 甲 | 乙 |
| 元素符号 | ①Na | ②Cl |
| 原子结构 示意图 |  | ③  |
| 周期 | 三 | 三 |
| 族 | ④IA | VII A |
 .
.(3)乙元素最高价氧化物对应水化物的化学式为HClO4.
(4)甲单质与水反应的化学方程式为2Na+2H2O=2NaOH+H2↑.
14.下列关于氧化物的各项叙述正确的是( )
| A. | 非金属氧化物肯定是酸性氧化物 | |
| B. | 碱性氧化物肯定是金属氧化物 | |
| C. | 金属氧化物都是碱性氧化物 | |
| D. | 不能跟酸反应的氧化物一定能跟碱反应 |
11.下列描述正确的是( )
| A. | 乙烷中若混有乙烯,可通过酸性高锰酸钾溶液除去 | |
| B. | 乙醇中是否混有水,可用加入金属钠是否产生气体进行检验 | |
| C. | 蚕丝和棉花的组成元素相同,分子结构不同,因而性质不同 | |
| D. | 乙酸乙酯是否混有乙酸,可用加石蕊试液是否变红进行检测 |
12.如图表示向AlCl3溶液滴加NaOH溶液过程中铝元素存在的微粒关系曲线不正确的是( )


| A. | AB线表示Al3+的物质的量的变化 | B. | OC表示AlO2-的物质的量的变化 | ||
| C. | CD线表示Al(OH)3的物质的量的变化 | D. | BE线表示AlO2-的物质的量的变化 |
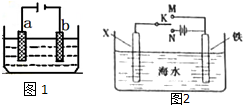 电化学原理在工业生产中有重要应用.如图1所示电解池中:
电化学原理在工业生产中有重要应用.如图1所示电解池中: