题目内容
一定温度下的密闭容器中存在如下反应:CO(g)+H2O(g)?CO2(g)+H2(g),已知CO(g)和H2O(g)的起始浓度均为2mol?L-1,经测定该反应在该温度下的平衡常数K=1,试判断:
(1)当CO转化率为25%时,该反应是否达到平衡,若未达到,向哪个方向进行?
(2)当CO的起始浓度仍为2mol?L-1,H2O(g)的起始浓度为6mol?L-1,求平衡时CO的转化率?
(1)当CO转化率为25%时,该反应是否达到平衡,若未达到,向哪个方向进行?
(2)当CO的起始浓度仍为2mol?L-1,H2O(g)的起始浓度为6mol?L-1,求平衡时CO的转化率?
考点:化学平衡的计算
专题:化学平衡专题
分析:(1)根据化学反应进行到某个状态时的浓度熵和化学平衡常数之间的大小关系来回答;
(2)温度不变时,K不变为1,根据三段式计算平衡时CO的浓度,再计算物质的转化率.
(2)温度不变时,K不变为1,根据三段式计算平衡时CO的浓度,再计算物质的转化率.
解答:
解:(1)当CO转化率为25%时,
CO(g)+H2O(g)?CO2(g)+H2(g)
初始浓度:2 2 0 0
变化浓度:0.5 0.5 0.5 0.5
末态浓度:1.5 1.5 0.5 0.5
此时浓度熵Qc=
=
<1,所以不是平衡状态,化学反应会向正向进行.
答:不是平衡状态,会向正方向进行;
(2)当CO的起始浓度仍为2mol?L-1,H2O(g)的起始浓度为6mol?L-1,设平衡时CO的转化的浓度为xmol?L-1,
CO(g)+H2O(g)?CO2(g)+H2(g)
初始浓度:2 6 0 0
变化浓度:x x x x
末态浓度:2-x 6-x x x
则
=1,解得x=1.5,所以CO的转化率为
×100%=75%,
答:平衡时CO的转化率为75%.
CO(g)+H2O(g)?CO2(g)+H2(g)
初始浓度:2 2 0 0
变化浓度:0.5 0.5 0.5 0.5
末态浓度:1.5 1.5 0.5 0.5
此时浓度熵Qc=
| 0.5×0.5 |
| 1.5×1.5 |
| 1 |
| 9 |
答:不是平衡状态,会向正方向进行;
(2)当CO的起始浓度仍为2mol?L-1,H2O(g)的起始浓度为6mol?L-1,设平衡时CO的转化的浓度为xmol?L-1,
CO(g)+H2O(g)?CO2(g)+H2(g)
初始浓度:2 6 0 0
变化浓度:x x x x
末态浓度:2-x 6-x x x
则
| x2 |
| (2-x)(6-x) |
| 1.5 |
| 2 |
答:平衡时CO的转化率为75%.
点评:本题考查了化学平衡的计算、化学平衡常数以及转化率的计算知识,把握三段式的计算方法的应用是关键,题目难度中等,侧重于计算能力的考查.

练习册系列答案
相关题目
某有机物A的分子式为C6H12O2,已知A~E有如图转化关系.则A的结构可能有( )
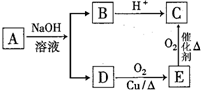

| A、1种 | B、2种 | C、3种 | D、4种 |
以下对核外电子运动状况的描述正确的是( )
| A、同一原子中,2p,3p,4p能级的轨道依次增多,均为哑铃状 |
B、当碳原子的核外电子排布由 转变为 转变为 时,这一过程中释放能量 时,这一过程中释放能量 |
| C、3p2表示3p能级有两个轨道 |
| D、在同一能级上运动的电子,其运动状态完全相同 |
C(石墨)=C(金刚石),△H=+1.895kJ/mol,相同条件下,下列说法正确的是( )
| A、石墨比金刚石稳定 |
| B、金刚石比石墨稳定 |
| C、相同物质的量的石墨比金刚石的总能量高 |
| D、两者互为同位素 |
能把Na2SO4、NH4NO3、KCl、(NH4)2SO4、CuSO4五瓶溶液加以区别的一种试剂是(必要时可以加热)( )
| A、BaCl2 |
| B、NaOH |
| C、AgNO3 |
| D、Ba(OH)2 |
 (1)可用如图示的方法表示不同反应类型之间的关系.如分解反应和氧化还原反应可表示为如图.请在下面的方框中画出离子反应、置换反应和氧化还原反应三者之间的关系.
(1)可用如图示的方法表示不同反应类型之间的关系.如分解反应和氧化还原反应可表示为如图.请在下面的方框中画出离子反应、置换反应和氧化还原反应三者之间的关系.