题目内容
12.A、B、C、D四种物质都含有一种共同的元素,A是常见的金属,C的溶液呈现黄色,A、B、C、D之间有如图所示转化关系.试回答下列问题:
(1)A是Fe,C是FeCl3.
(2)C的溶液与NaOH溶液混合后产生的现象是有红褐色沉淀生成.
(3)反应①的反应类型是置换反应.
分析 A是常见的金属,与氯气反应生成C,C的溶液呈现黄色,且C与KSCN溶液混合溶液为血红色,则C含有Fe3+,由元素守恒可知A为Fe,结合转化关系可知,C为FeCl3,B为FeCl2,据此解答.
解答 解:A是常见的金属,与氯气反应生成C,C的溶液呈现黄色,且C与KSCN溶液混合溶液为血红色,则C含有Fe3+,由元素守恒可知A为Fe,结合转化关系可知,C为FeCl3,B为FeCl2.
(1)由上述分析可知,A为Fe,C为FeCl3,故答案为:Fe;FeCl3;
(2)C为FeCl3,与NaOH溶液反应为FeCl3+3NaOH=Fe(OH)3↓+3NaCl,有红褐色沉淀生成,
故答案为:有红褐色沉淀生成;
(3)反应①为Fe+2HCl=FeCl2+H2↑,为置换反应,故答案为:置换反应.
点评 本题考查无机物的推断,C与KSC溶液呈血红色是推断的突破口,明确铁离子的颜色及检验方法是解答本题的关键,题目难度不大.

练习册系列答案
相关题目
2.能正确表示下列反应的离子方程式为( )
| A. | 向明矾溶液中滴加Ba(OH)2溶液,恰好使SO${\;}_{4}^{2-}$沉淀完全2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ | |
| B. | 铝溶于氢氧化钠溶液:Al+2OH-+H2O═AlO2-+H2↑ | |
| C. | 玻璃试剂瓶被烧碱溶液腐蚀:SiO2+2Na++2OH-═Na2SiO3↓+H2O | |
| D. | VO2+与酸性高锰酸钾溶液反应:5VO2++MnO${\;}_{4}^{-}$+H2O═5VO${\;}_{2}^{+}$+Mn2++2H+ |
20.四种仪器中,不能用来加热的是( )
| A. |  烧杯 | B. |  容量瓶 | C. |  试管 | D. |  烧瓶 |
7.下列物质中,属于电解质是( )
| A. | 铜丝 | B. | NaCl | C. | 酒精 | D. | 蔗糖 |
4.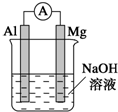 将镁条、铝条平行插入一定浓度的NaOH溶液中,用导线和电流表连接成原电池.装置如图所示,此电池工作时,下列叙述中正确的是( )
将镁条、铝条平行插入一定浓度的NaOH溶液中,用导线和电流表连接成原电池.装置如图所示,此电池工作时,下列叙述中正确的是( )
 将镁条、铝条平行插入一定浓度的NaOH溶液中,用导线和电流表连接成原电池.装置如图所示,此电池工作时,下列叙述中正确的是( )
将镁条、铝条平行插入一定浓度的NaOH溶液中,用导线和电流表连接成原电池.装置如图所示,此电池工作时,下列叙述中正确的是( )| A. | Mg比Al活泼,Mg失去电子被氧化成Mg2+ | |
| B. | 铝条表面虽有氧化膜,但可不必处理 | |
| C. | 正极反应式为2H++2e-═H2↑ | |
| D. | Al是电池负极,开始工作时溶液中会立即有白色沉淀析出 |

 室温时,向100mL 0.1mol/L NH4HSO4溶液中滴加0.1mol/L NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示.
室温时,向100mL 0.1mol/L NH4HSO4溶液中滴加0.1mol/L NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示.