题目内容
15.下列分子中,所有原子都满足最外层为8电子结构的是( )| A. | COCl2 | B. | SiH4 | C. | SF6 | D. | PCl5 |
分析 对于ABn型共价化合物元素化合价绝对值+元素原子的最外层电子层=8,则该元素原子满足8电子结构,含H元素的化合物一定不满足8电子结构.
解答 解:A.COCl2中C元素化合价为+4,C原子最外层电子数为4,所以4+4=8,C原子满足8电子结构;O元素化合价为-2,O原子最外层电子数为6,所以2+6=8,O原子满足8电子结构;Cl元素化合价为-1,Cl原子最外层电子数为7,所以1+7=8,Cl原子满足8电子结构,都满足8电子稳定结构,故A正确;
B.SiH4中Si元素化合价为+4,Si原子最外层电子数为4,所以4+4=8,Si原子满足8电子结构,H原子的最外层电子为:1+1=2,不都满足8电子稳定结构,故B错误;
C.SF6中S元素化合价为+6,S原子最外层电子数为6,所以6+6=12,S原子不满足8电子结构,F元素化合价为-1,F原子最外层电子数为7,所以1+7=8,F原子满足8电子结构,故C错误;
D.PCl5中,P原子的最外层电子为:5+5=10,Cl原子的最外层电子为:7+|-1|=8,不都满足8电子稳定结构,故D错误.
故选:A.
点评 本题考查原子的结构,本题中注意判断是否满足8电子结构的方法,注意利用化合价与最外层电子数来分析即可解答,明确所有原子都满足最外层8电子结构是解答的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
20.下列说法中不正确的是( )
| A. | 向卤代烃的水解液中直接加入 AgNO3溶液,可以确定卤代烃中卤元素 | |
| B. | CH2Cl2的结构只有一种证明 CH4是正四面体结构而不是平面正方形结构 | |
| C. | 通过石油化学工业中的催化重整等工艺可以获得芳香烃 | |
| D. | 邻二氯苯不存在同分异构体说明苯分子中 6个碳原子之间的键是一样的 |
5.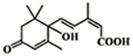 大量盆栽鲜花因施用了S-诱抗素制剂,得以保证鲜花盛开,S-诱抗素的分子结构如图,下列关于该分子的说法正确的是( )
大量盆栽鲜花因施用了S-诱抗素制剂,得以保证鲜花盛开,S-诱抗素的分子结构如图,下列关于该分子的说法正确的是( )
 大量盆栽鲜花因施用了S-诱抗素制剂,得以保证鲜花盛开,S-诱抗素的分子结构如图,下列关于该分子的说法正确的是( )
大量盆栽鲜花因施用了S-诱抗素制剂,得以保证鲜花盛开,S-诱抗素的分子结构如图,下列关于该分子的说法正确的是( )| A. | 1mol该物质与足量的NaOH溶液反应最多消耗2mol NaOH | |
| B. | 该物质在Cu作催化剂条件下能被催化氧化 | |
| C. | 该物质能发生氧化、还原、取代反应 | |
| D. | 分别与足量的Na、NaHCO3 反应生成的气体在相同状况下体积比为2:1 |
 硝酸工业是国民经济的命脉产业,工业制硝酸通常是如下过程
硝酸工业是国民经济的命脉产业,工业制硝酸通常是如下过程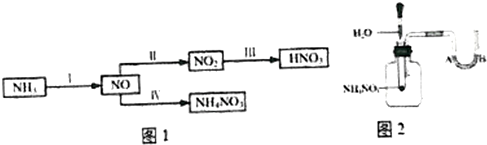

 .
. .
. .
. .
.