题目内容
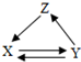
对由X、Y元素形成的化合物X2Y2的叙述正确的是( )
| A、若是离子化合物,则阳阴离子个数比肯定不等于1:1 |
| B、若该化合物有Y-Y键,则肯定是共价化合物 |
| C、若溶于水时有X-Y键的断裂,则肯定是强电解质 |
| D、若X、Y原子间的共价键键能大,则熔、沸点肯定高 |
考点:原子结构与元素的性质
专题:元素周期律与元素周期表专题
分析:A.化学式用构成物质粒子的最简比表示;
B.若X2Y2为Na2O2,存在O-O键;
C.弱电解质在溶液中也可以发生电离;
D.分子晶体的熔点与共价键无关.
B.若X2Y2为Na2O2,存在O-O键;
C.弱电解质在溶液中也可以发生电离;
D.分子晶体的熔点与共价键无关.
解答:
解:A.化学式用构成物质粒子的最简比表示,若为是离子化合物,则阳阴离子个数比肯定不等于1:1,若阳阴离子个数比等于1:1,则为XY,故A正确;
B.若X2Y2为Na2O2,存在O-O键,所以若该化合物有Y-Y键,则也可能是离子化合物,故B错误;
C.化学键断裂与强弱电解质无关,弱电解质在溶液中也可以发生断键而电离,故C错误;
D.该物质若为分子晶体,分子晶体的熔沸点与分子间作用力有关,共价键不影响物质的熔沸点,故D错误;
故选A.
B.若X2Y2为Na2O2,存在O-O键,所以若该化合物有Y-Y键,则也可能是离子化合物,故B错误;
C.化学键断裂与强弱电解质无关,弱电解质在溶液中也可以发生断键而电离,故C错误;
D.该物质若为分子晶体,分子晶体的熔沸点与分子间作用力有关,共价键不影响物质的熔沸点,故D错误;
故选A.
点评:本题考查了原子结构与性质关系,题目难度中等,B选项注意利用常见物质进行列举判断.

练习册系列答案
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目
溶液中氧化剂XO3-的含量有3×10-2mol,与300mL 0.2mol?L-1亚硫酸钠(Na2SO3)溶液恰好反应完全,已知Na2SO3被氧化为Na2SO4,则还原产物中元素X的价态是( )
| A、+2 | B、-2 | C、+1 | D、0 |
下列各组离子一定能大量共存的是( )
| A、加入KSCN溶液显血红色的溶液中:Fe2+、Mg2+、Cl-、SO42- |
| B、能与金属铝反应放出氢气的溶液中:K+、NO3-、Cl-、Fe2+ |
| C、常温下水电离出的c(H+)?c(OH-)=10-20 (mol?L-1)2的溶液中:Na+、ClO-、S2-、NH4+ |
| D、在AlCl3溶液中,Na+、AlO2-、NO3-、SO42- |
下列关于酸、碱、盐、氧化物的元素组成的说法中,正确的是( )
| A、酸、碱一定含有氢,盐一定不含氢 |
| B、碱、盐可能含氧,酸一定含氧 |
| C、酸、碱、盐可能都不含金属元素 |
| D、金属氧化物一定是碱性氧化物 |
下列有关实验操作或仪器的使用正确的是( )
A、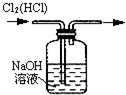 除去氯气中的氯化氢 |
B、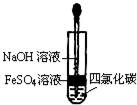 制备Fe(OH)2 |
C、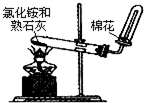 实验室制备氨气 |
D、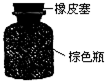 保存浓硝酸 |