题目内容
把Ca(OH)2放入一定量的蒸馏水中,一定温度下达到溶解平衡:Ca(OH)2(s)=Ca2++2OH-.当向悬浊液中加入少量生石灰后,若温度不变,下列判断正确的是( )
| A、溶液中Ca2+数目减少 |
| B、Ca2+浓度增大 |
| C、溶液中OH-浓度减小 |
| D、溶液OH-浓度增大 |
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:向悬浊液中加少量生石灰,发生:CaO+H2O=Ca(OH)2,消耗水,溶液c(Ca2+)、c(OH-)增大,由于原溶液已达到饱和,则平衡向逆反应方向移动,以此解答该题.
解答:
解:向悬浊液中加少量生石灰,发生:CaO+H2O=Ca(OH)2,
A.加入CaO,消耗水,由于原溶液已达到饱和,则平衡向逆反应方向移动,溶液中Ca2+数目减少,故A正确;
B.反应后仍为饱和溶液,c(Ca2+)不变,故B错误;
C.反应后仍为饱和溶液,c(OH-)不变,溶液pH不变,故C错误;
D.反应后仍为饱和溶液,c(OH-)不变,溶液pH不变,故D错误;
故选A.
A.加入CaO,消耗水,由于原溶液已达到饱和,则平衡向逆反应方向移动,溶液中Ca2+数目减少,故A正确;
B.反应后仍为饱和溶液,c(Ca2+)不变,故B错误;
C.反应后仍为饱和溶液,c(OH-)不变,溶液pH不变,故C错误;
D.反应后仍为饱和溶液,c(OH-)不变,溶液pH不变,故D错误;
故选A.
点评:本题考查难溶电解质的溶解平衡,题目难度中等,本题注意向悬浊液中加少量生石灰,发生:CaO+H2O=Ca(OH)2,从平衡移动的角度分析.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
已知Ksp(Ag2CrO4)=9.0×10-12,将等体积的4×10-3mol?L-1的AgNO3溶液和4×10-3mol?L-1的K2CrO4溶液混合,下列说法正确的是( )
| A、恰好形成Ag2CrO4饱和溶液 |
| B、能析出Ag2CrO4沉淀 |
| C、不能析出Ag2CrO4沉淀 |
| D、无法确定能否析出Ag2CrO4沉淀 |
下列说法正确的是( )
| A、海南岛四面环海,水资源丰富,不必节约用水 |
| B、明矾既能沉降水中的悬浮物,又能杀菌消毒 |
| C、可通过长期饮用含Ca2+浓度较高的水来补钙 |
| D、若不慎接触敌敌畏或甲胺磷,最好用碱性肥皂液清洗 |
①已知t℃时AgCI的Ksp=2×10-10;②在t℃时Ag2CrO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )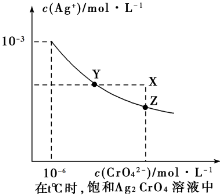

| A、在t℃时,Ag2CrO4的Ksp为1×10-9 |
| B、在饱和Ag2CrO4溶液中加入K2CrO4可使溶液由Y点到X点 |
| C、在t℃时,以0.01 mol/LAgNO3溶液滴定20 mL 0.01 mol/LKCI和0.01 mol/L的K2CrO4的混和溶液,CrO42-先沉淀 |
| D、在t℃时,反应Ag2CrO4(s)+2 Cl-(aq)?2AgCl(s)+CrO42-(aq)的平衡常数K=2.5×107 |
如图所示的实验操作中正确的是( )
A、 二氧化碳的验满 |
B、 稀释浓硫酸 |
C、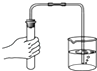 检查气密性 |
D、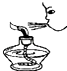 熄灭酒精灯 |
关于中和热测定的说法错误的是( )
| A、实验需用到的主要玻璃仪器包括大、小烧杯,温度计,环形玻璃搅拌棒及泡沫塑料板、碎泡沫塑料(或硬纸板、碎纸条)等 |
| B、盐酸与某强碱中和放出的热量随反应物用量的改变而改变,但中和热不变 |
| C、NaOH稍过量的目的是保证盐酸完全被NaOH中和 |
| D、测定结果准确与否的关键是尽量减小热量损失及准确读取混合溶液的最高温度等 |
实验中需要2mol?L-1的Na2CO3溶液950mL,配制时,你认为应该选用的容量瓶的规格和称取的碳酸钠质量分别是( )
| A、1000 mL,212 g |
| B、950 mL,201.4 g |
| C、500 mL,286 g |
| D、任意规格,572 g |
