题目内容
下列根据实验操作和现象所得出的结论正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 用铂丝蘸取少量某无色溶液进行焰色反应 | 火焰呈黄色 | 该溶液一定是钠盐溶液 |
| B | 向浓度均为0.1mol?L-1 NaCl和NaI混合溶液中滴加少量AgNO3溶液 | 出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| C | 向溶液X中先滴加稀硝酸,再滴加Ba(NO3)2溶液 | 出现白色沉淀 | 溶液X 中一定含有SO42- |
| D | 向淀粉水解液中加入新制Cu(OH)2,煮沸 | 没有生成砖红色沉淀 | 淀粉未水解 |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价
专题:实验评价题
分析:A.只能说明含有钠元素;
B.同类型的沉淀,溶度积小的沉淀先析出;
C.亚硫酸根离子具有还原性,能被稀硝酸氧化为硫酸根离子;
D.葡萄糖在碱性条件下与新制Cu(OH)2浊液反应.
B.同类型的沉淀,溶度积小的沉淀先析出;
C.亚硫酸根离子具有还原性,能被稀硝酸氧化为硫酸根离子;
D.葡萄糖在碱性条件下与新制Cu(OH)2浊液反应.
解答:
解:A.只能说明含有钠元素,不一定为钠盐,可能为碱溶液,故A错误;
B.同类型的沉淀,溶度积小的沉淀先析出,即Ksp(AgCl)>Ksp(AgI),故B正确;
C.溶液X 中滴加稀硝酸,生成硫酸根离子,滴加Ba(NO3)2溶液时生成硫酸钡白色沉淀,则溶液X中含有SO42-或SO32-,故C错误;
D.葡萄糖与新制Cu(OH)2浊液反应需在碱性条件下,应加入碱将水解后的淀粉溶液调节成碱性,才可以产生砖红色沉淀,故D错误.
故选B.
B.同类型的沉淀,溶度积小的沉淀先析出,即Ksp(AgCl)>Ksp(AgI),故B正确;
C.溶液X 中滴加稀硝酸,生成硫酸根离子,滴加Ba(NO3)2溶液时生成硫酸钡白色沉淀,则溶液X中含有SO42-或SO32-,故C错误;
D.葡萄糖与新制Cu(OH)2浊液反应需在碱性条件下,应加入碱将水解后的淀粉溶液调节成碱性,才可以产生砖红色沉淀,故D错误.
故选B.
点评:本题考查较为综合,涉及物质的检验、难溶电解质的溶解平衡等知识,为高考常见题型和高频考点,侧重于学生的分析能力、实验能力和评价能力的考查,注意把握实验操作要点,结合物质的性质综合考虑,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
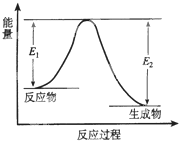 反应A(g)+B(g)?C(g)+D(g) 发生过程中的能量变化如右图,△H 表示反应的焓变.下列说法正确的是( )
反应A(g)+B(g)?C(g)+D(g) 发生过程中的能量变化如右图,△H 表示反应的焓变.下列说法正确的是( )| A、该反应为吸热反应 |
| B、反应体系中加入催化剂,反应速率增大,E1减小,E2增大 |
| C、反应体系中加入催化剂,反应速率增大,△H不变 |
| D、反应达到平衡时,降低温度,A的转化率增大 |
下列说法正确的是( )
| A、族序数等于其周期序数的元素一定是金属元素 |
| B、13C与14C互为同位素,它们的化学性质相同,但相对原子质量不同 |
| C、元素原子的最外层电子数等于元素的最高化合价 |
| D、全部由非金属元素组成的化合物中只含共价键 |
已知:氢氧化镁能溶于浓度均为3mol/L的①盐酸②NH4Cl溶液③醋酸铵溶液(中性),下列说法正确的是( )
| A、c(NH4+):③>② |
| B、pH:①>②>③ |
| C、Mg(OH)2溶于②的主要原因是由于NH4+水解使溶液显酸性,导致平衡Mg(OH)2(s)?Mg2+(aq)+2OH-(aq)向溶解方向移动 |
| D、等体积①和③混合溶液中 c(Cl-)>c(NH4+)>c(H+)>c(CH3COO-)>c(OH-) |
下列有关表示正确的是( )
A、氯离子的结构示意图: |
B、氯化氢分子的电子式: |
| C、乙烯分子的结构式:CH2=CH2 |
D、苯分子的比例模型: |
下列与化学反应能量变化相关的叙述正确的是( )
| A、放热反应的反应速率总是大于吸热反应的反应速率 |
| B、同温同压下,反应H2(g)+Cl2(g)═2HCl (g)在光照和点燃条件下的△H相同 |
| C、甲烷的燃烧热为890.3kJ/mol,则甲烷燃烧的热化学方程式为 CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3kJ/mol |
| D、相同条件下,2mol氢原子所具有的能量小于1mol氢分子所具有的能量 |
2.24g铁屑与30mL 2mol/L盐酸充分反应后,溶液中FeCl2的物质的量是( )
| A、0.02 mol |
| B、0.03 mol |
| C、0.04mol |
| D、0.06 mol |
下列物质中,既能与盐酸反应,又能与NaOH溶液反应的是( )
①NaHCO3 ②AgNO3③(NH4)2S ④HOOC-COONa⑤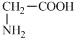 ⑥
⑥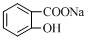
①NaHCO3 ②AgNO3③(NH4)2S ④HOOC-COONa⑤
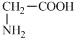 ⑥
⑥
| A、全部 | B、①②④⑤⑥ |
| C、②③④⑤⑥ | D、②④⑤⑥ |
已知:2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ?mol-1 H2(g)+
O2(g)═H2O(l)△H=-285.8kJ?mol-1由此可知,在等温下蒸发45g液态水需吸收的热量( )
| 1 |
| 2 |
| A、483.6 kJ |
| B、110 kJ |
| C、285.8 kJ |
| D、221 kJ |