题目内容
10.下列物质中,能够导电的电解质是( )| A. | 氨水 | B. | 蔗糖 | C. | 铜导线 | D. | 熔融的KCl |
分析 电解质是在溶液中或熔融状态下能够导电的化合物,电解质必须为化合物,则由于溶液为混合物,所以能够导电的电解质必须为熔融离子化合物,据此进行解答.
解答 解:A.氨水为混合物,不属于电解质,故A错误;
B.蔗糖的水溶液不导电,为非电解质,故B错误;
C.铜为单质,不属于电解质和非电解质,故C错误;
D.熔融氯化钾能够导电,且为电解质,故D正确;
故选D.
点评 本题考查了电解质及导电性的判断,题目难度不大,明确电解质的概念为解答关键,试题侧重基础知识的考查,培养了学生的灵活应用能力.

练习册系列答案
相关题目
15.分类法是学习和研究化学的一种常用的科学方法.下列分类合理的是( )
①Fe2O3、CaO、Al2O3都是碱性氧化物
②根据反应中是否有氧气参加,将化学反应分为氧化还原反应和非氧化还原反应
③根据元素原子最外层电子数的多少将元素分为金属元素和非金属元素
④根据纯净物中是否含氧元素,来判断是否属于氧化物
⑤根据分散系的稳定性将分散系分为胶体、溶液和浊液.
①Fe2O3、CaO、Al2O3都是碱性氧化物
②根据反应中是否有氧气参加,将化学反应分为氧化还原反应和非氧化还原反应
③根据元素原子最外层电子数的多少将元素分为金属元素和非金属元素
④根据纯净物中是否含氧元素,来判断是否属于氧化物
⑤根据分散系的稳定性将分散系分为胶体、溶液和浊液.
| A. | 只有①②④ | B. | 只有③⑤ | C. | 只有④ | D. | 都不对 |
1.某元素X的最高正化合价为+7价,下面的叙述不正确的是( )
| A. | 该元素的原子最外层上有7个电子 | |
| B. | 该元素最高价氧化物的化学式为XO3 | |
| C. | 该元素位于ⅦA族 | |
| D. | 该元素最高价氧化物对应水化物的化学式为HXO4 |
18.${\;}_{55}^{137}$Cs是核反应堆的常见放射性副产物,${\;}_{55}^{137}$Cs能自发转化为${\;}_{56}^{137}$Ba,同时放出射线.下列有关叙述正确的是( )
| A. | ${\;}_{55}^{137}$Cs与${\;}_{56}^{137}$Ba互为同位素 | |
| B. | ${\;}_{55}^{137}$Cs与${\;}_{56}^{137}$Ba中子数相等 | |
| C. | ${\;}_{56}^{137}$Ba原子最外层电子数为2 | |
| D. | Ba比Cs更容易失去电子 |
5.下列叙述错误的是( )
| A. | 1mol任何物质都含有6.02×1023个原子 | |
| B. | 0.012kg12C 含有阿伏加德罗常数个碳原子 | |
| C. | 在使用摩尔表示物质的量的单位时,应指明粒子的种类 | |
| D. | 物质的量是国际单位制中七个基本物理量之一 |
15.考古中常利用${\;}_{6}^{14}$C测定一些文物的年代.${\;}_{6}^{14}$C和${\;}_{6}^{12}$C的关系为( )
| A. | 同种核素 | B. | 同位素 | C. | 同素异形体 | D. | 同种分子 |
2.仪器名称为“容量瓶”的是( )
| A. | 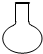 | B. |  | C. | 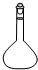 | D. |  |
19.已知HA、H2B为二种弱酸,HA的电离常数为KHA,H2B的电离常数为K1、K2,其大小依次是K1>KHA>K2,由此可以推测以下各反应中不能进行的是( )
| A. | NaA+H2B→NaHB+HA | B. | 2NaA+H2B→Na2B+2HA | ||
| C. | NaHB+HA→NaA+H2B | D. | Na2B+HA→NaHB+NaA |
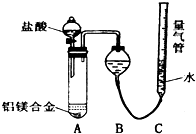 铝镁合金已成为轮船制造、化工生产等行业的重要材料.研究性学习小组的三位同学,为测定某含镁3%一5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列三种不同实验方案进行探究.填写下列空白.
铝镁合金已成为轮船制造、化工生产等行业的重要材料.研究性学习小组的三位同学,为测定某含镁3%一5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列三种不同实验方案进行探究.填写下列空白.