题目内容
下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:
(1)由①、③、⑧三种元素形成的离子化合物的电子式为______;由②、④两元素构成的三原子分子的极性为______.
(2)⑥的原子结构示意图为______;⑦的氧化物的晶体类型是______.
(3)②、③、⑦最高价含氧酸的酸性由弱到强的顺序是______.
(4)④、⑤、⑧三种元素可形成“84”消毒液的有效成分,写出该化合物中存在的化学键的类型为______.
| 族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 1 | ① | ||||||
| 2 | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | |||
(2)⑥的原子结构示意图为______;⑦的氧化物的晶体类型是______.
(3)②、③、⑦最高价含氧酸的酸性由弱到强的顺序是______.
(4)④、⑤、⑧三种元素可形成“84”消毒液的有效成分,写出该化合物中存在的化学键的类型为______.
由元素在周期表中的位置可知,①为H,②为C,③为N,④为O,⑤为Na,⑥为Al,⑦为Si,⑧为Cl.
(1)①、③、⑧三种元素形成的离子化合物为氯化铵,其电子式为
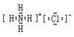
,②、④两元素构成的三原子分子为CO2,结构对称,正负电荷的中心重合,为非极性分子,
故答案为:
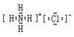
;非极性分子;
(2)Al的原子序数为13,其原子结构示意图为

,⑦的氧化物为SiO2,是由原子以共价键结合具有网状结构的原子晶体,
故答案为:

;原子晶体;
(3)非金属性越强,最高价含氧酸的酸性越强,非金属性为N>C>Si,所以最高价含氧酸的酸性由弱到强的顺序是H2SiO3<H2CO3<HNO3,故答案为:H2SiO3<H2CO3<HNO3;
(4)④、⑤、⑧三种元素可形成“84”消毒液的有效成分为NaClO,含有离子键和极性共价键,故答案为:离子键、极性共价键.
(1)①、③、⑧三种元素形成的离子化合物为氯化铵,其电子式为
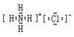
,②、④两元素构成的三原子分子为CO2,结构对称,正负电荷的中心重合,为非极性分子,
故答案为:
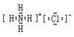
;非极性分子;
(2)Al的原子序数为13,其原子结构示意图为

,⑦的氧化物为SiO2,是由原子以共价键结合具有网状结构的原子晶体,
故答案为:

;原子晶体;
(3)非金属性越强,最高价含氧酸的酸性越强,非金属性为N>C>Si,所以最高价含氧酸的酸性由弱到强的顺序是H2SiO3<H2CO3<HNO3,故答案为:H2SiO3<H2CO3<HNO3;
(4)④、⑤、⑧三种元素可形成“84”消毒液的有效成分为NaClO,含有离子键和极性共价键,故答案为:离子键、极性共价键.

练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目








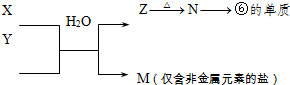
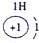
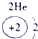
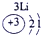
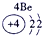
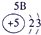
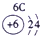
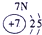
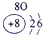
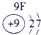
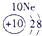
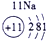





 表示的是
表示的是