题目内容
16.下列化学方程式不能用离子方程式2H++CO32-=H2O+CO2↑表示的是( )| A. | 2HCl+Na2CO3═2NaCl+H2O+CO2↑ | B. | 2HNO3+BaCO3═Ba(NO3)2+H2O+CO2↑ | ||
| C. | H2SO4+Na2CO3═Na2SO4+H2O+CO2↑ | D. | H2SO4+(NH4)2CO3═(NH4)2SO4+H2O+CO2↑ |
分析 2H++CO32-=H2O+CO2↑表示可溶性的碳酸盐和强酸之间反应生成可溶性的盐、水以及二氧化碳的反应,结合离子反应中保留化学式的物质来解答.
解答 解:A、C、D的离子反应均为2H++CO32-=H2O+CO2↑,只有B的离子反应为2H++BaCO3=Ba2++H2O+CO2↑,
故选B.
点评 本题考查离子反应方程式的书写及意义,为高频考点,把握离子反应方程式的书写方法为解答的关键,侧重复分解反应的离子反应考查,注意离子反应中保留化学式的物质,题目难度不大.

练习册系列答案
相关题目
17.已知反应:2NO2+2NaOH═NaNO3+NaNO2+H2O;NO+NO2+2NaOH═2NaNO2+H2O
现有XmolNO2和YmolNO(X>Y)组成的混合气体,欲用m L含nmolNaOH的溶液吸收,使该混合气体全部转化成盐(NaNO3和NaNO2)进入溶液,则n的值至少是( )
现有XmolNO2和YmolNO(X>Y)组成的混合气体,欲用m L含nmolNaOH的溶液吸收,使该混合气体全部转化成盐(NaNO3和NaNO2)进入溶液,则n的值至少是( )
| A. | X/m mol | B. | 2X/3mol | C. | (X+Y)mol | D. | 2(X+Y)/3mol |
4.已知:
②
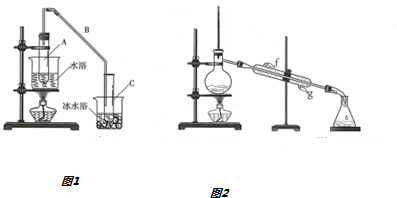
某化学小组采用如图1所示装置,用环乙醇制备环乙烯.
(1)制备粗品将12.5mL环乙醇加入试管A中,在加入1mL浓硫酸,摇匀,放入碎瓷片,缓慢加热至反应完全,在试管C内得到环乙烯粗品.试管C置于冰水浴中的目的是使环己烯液化,减少挥发.
(2)制备精品
①环乙烯粗品中含有环乙醇和少量有机酸性杂质等.加入饱和食盐水,振荡、静置、分层,环乙烯在上层(填“上”或“下”)层,分液后用c(填字母序号)洗涤.
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
②再次分液,并用无水氯化钙干燥,过滤后再按图2装置蒸馏,冷凝水从g(填字母)口进入
③收集产品时,控制的温度应在83℃,实验制得的环乙烯精品质量低于理论产量,可能的原因是B(填字母序号)
A.蒸馏时从70℃开始收集产品
B.制备粗品时环乙醇随产品一起蒸出.

②
| 密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
| 环乙醇 | 0.96 | 25.93 | 161 | 能溶于水 |
| 环乙烯 | 0.81 | -103 | 83 | 难溶于水 |
(1)制备粗品将12.5mL环乙醇加入试管A中,在加入1mL浓硫酸,摇匀,放入碎瓷片,缓慢加热至反应完全,在试管C内得到环乙烯粗品.试管C置于冰水浴中的目的是使环己烯液化,减少挥发.

(2)制备精品
①环乙烯粗品中含有环乙醇和少量有机酸性杂质等.加入饱和食盐水,振荡、静置、分层,环乙烯在上层(填“上”或“下”)层,分液后用c(填字母序号)洗涤.
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
②再次分液,并用无水氯化钙干燥,过滤后再按图2装置蒸馏,冷凝水从g(填字母)口进入
③收集产品时,控制的温度应在83℃,实验制得的环乙烯精品质量低于理论产量,可能的原因是B(填字母序号)
A.蒸馏时从70℃开始收集产品
B.制备粗品时环乙醇随产品一起蒸出.
11.光纤通信70年代后期发展起来的一种新型通信技术,目前长距离光纤通信系统已投入使用,光纤通信的光导纤维是由下列哪种物质经特殊工艺制成的( )
| A. | SiC | B. | SiO2 | C. | Si | D. | Si3N4 |
1.某元素原子的质量数为52,中子数为28,其基态原子未成对电子数为( )
| A. | 6 | B. | 5 | C. | 4 | D. | 1 |
8.下列关于NO的叙述正确的是( )
| A. | 常温常压下,含等质量氧元素的NO和CO的体积相等 | |
| B. | NO是一种有刺激性气味的红棕色气体 | |
| C. | NO易溶于水,所以可用排空气法收集 | |
| D. | NO不能通过化合反应获得 |
6.现在甲基、羟基、羧基、苯基四种原子团,两两组合形成化合物,其水溶液呈酸性的有( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |